Экспериментальное определение - коэффициент - активность
Cтраница 2
К сожалению, метод Льюиса не дает такой возможности. Он требует для каждого конкретного случая экспериментального определения коэффициентов активности каким-нибудь независимым методом или же использования табличных данных. Многие табличные коэффициенты активности рассчитаны из электрохимических измерений, поэтому, казалось бы, ими нельзя пользоваться для решения обратных задач - определения отклонения электрохимических систем от идеального состояния. На самом деле такие задачи решают часто и обоснованность применения табличных значений коэффициентов активности обусловлена тем, что во всех случаях, когда последние определяли несколькими независимыми методами, получали практически совпадающие друг с другом результаты. [16]
Метод вычисления коэффициента активности по экспериментальным данным [ см. уравнение (8.7) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [17]
Приведенный метод позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [18]
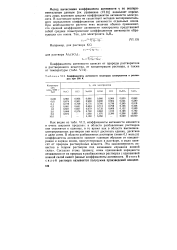 |
Коэффициенты активности некоторых электролитов в растворах при 298 К. [19] |
Метод вычисления коэффициента активности Y по экспериментальным данным [ см. уравнение (VI.8) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [20]
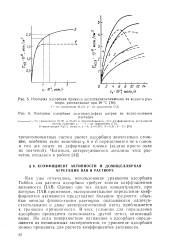 |
Изотерма адсорбции бромида цетилтриметиламмония из водного раствора, рассчитанная при 20 С.| Изотермы адсорбции додецилсульфата натрия из водно-солевого. [21] |
Как уже отмечалось, использование уравнения адсорбции Гиббса для расчета адсорбции требует знания коэффициентов активности ПАВ. Однако при тех малых концентрациях, при которых ПАВ применяют, экспериментальное определение коэффициентов активности представляет большие трудности: обычные методы физико-химии растворов оказываются малочувствительными и даже электрохимический метод приближается к границам применимости. В этих условиях для определения адсорбции приходится использовать другой метод, описанный выше. Но если поверхностное натяжение и адсорбция определяются из независимых экспериментов, то уравнение адсорбции. [22]
Коэффициенты активности относятся к составным частям системы. Считается, что они являются величинами переменными, зависящими от концентрации. Однако теоретически обоснованные методы экспериментального определения коэффициентов активности не разработаны. По смыслу они характеризуют отклонение реальных систем от идеального состояния, к которому применимы законы идеальных газов. Опыт показывает, что с уменьшением концентрации системы отклонение свойств ее от идеального состояния уменьшается. Поэтому считается, что при разбавлении состояние физико-химических систем приближается к идеальному и величины коэффициентов активности приближаются к единице. В реальных системах с конечными концентрациями составных частей коэффициенты активности отличны от единицы и бывают больше или меньше ее. [23]
Большой практический и научный интерес представляет задача количественного описания систем с водной фазой, содержащей несколько электролитов ( кислоты, высалива-тели и др.), требующая определения среднего ионного коэффициента активности распределяющегося электролита в водной фазе как функции ее состава, а во многих случаях также количественного учета процессов комплексообразования в водной фазе. Если стехиометрия процессов в органической фазе и константы экстракции известны, возможно также экспериментальное определение коэффициента активности извлекаемой соли в смешанном водном растворе. [24]
Страницы: 1 2