Экспериментальное определение - температура
Cтраница 2
Ввиду большого числа влияющих факторов и сложности экспериментального определения температуры поверхности частиц внутри слоя точность расчетных соотношений для коэффициентов межфазной теплоотдачи обычно не превышает 20 % для частиц правильной формы и 30 - 40 % для частиц существенно нерегулярной геометрической конфигурации. [16]
Таким образом, исследование взаимной растворимости двух жидкостей в зависимости от температуры заключается в экспериментальном определении температуры растворения ( расслоения) для смесей различных составов. На основании полученных данных строят график я координатах состав - температура. [17]
На рис. 13, а, б, в дан график сравнения результатов расчета по формуле ( 101) с данными экспериментального определения температуры жидкости в различных сечениях трубопровода при уменьшении температуры подогрева. В целом отмечается хорошее совпадение теории с экспериментом. Максимальное отклонение не превышает 3 С, что составляет 8 5 % измеренного значения температуры. Такое расхождение находится в пределах точности выполненных измерений. [18]
Поскольку для битумов дорожных марок трещиностойкость можно предсказать по номограммам, зная пенетрацию при 0 и 25 С, то отпадает необходимость в экспериментальном определении температур хрупкости по Фраасу или растрескивания по методу БашНИИНП, что следует учесть при стандартизации этих характеристик дорожных битумов. [19]
Однако для практического использования этого уравнения нужно располагать обширной информацией о свойствах растворов и растворителя, получение которой связано с большими трудностями, чем экспериментальное определение температуры кипения раствора. [20]
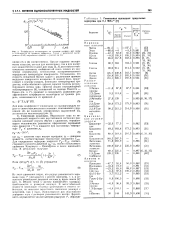 |
Коэффициент теплоотдачи на границе раздела для воды п зависимости от времени выдержки. Точки - результат эксперимента [ 38. штриховая кривая - расчет по ( 5. [21] |
Однако недавние эксперименты показали, что как для неполярных, так и для полярных жидкостей [1] и даже для воды [ 2, 3 [ достигаются максимальные величины; сообщения об очень низких их значениях определялись неточностями экспериментального определения температуры поверхности. Установлено, что скорость испарения быстро падает с увеличением времени выдержки поверхности испарения. В жидкой фазе, прилегающей к границе раздела, возникают температурные градиенты, чтобы обеспечить перенос скрытой теплоты результирующего потока пара. [22]
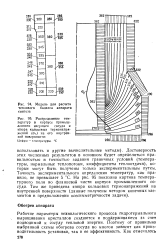 |
Модель для расчета теплового баланса аппарата синтеза.| Распределение температур в корпусе промышленного несущего сосуда и эпюра кольцевых термонапря-женнй ( at на его внутренней поверхности. [23] |
Достоверность этих численных результатов в основном будет определяться правильностью и точностью задания граничных условий ( температуры, нормальные теплопотоки, коэффициенты теплоотдачи), которые могут быть получены только экспериментальным путем. Точность экспериментального определения температур, как правило, не превышает 5 С. На рис. 95 показана картина температурного поля во фланцевой части корпуса промышленного сосуда. [24]
Как известно, температурой кристаллизации считают температуру, при которой первые зародыши кристаллов, находясь в термодинамическом равновесии с жидкостью, бесконечно разбавлены жидкой фазой. При экспериментальном определении температуры кристаллизации производят экстраполяцию кривых кристаллизации к граничной температуре, при которой появляются первые зародыши кристаллов в процессе затвердевания. Кривые кристаллизации в координатах: температура исследуемой системы Т - время / используют для определения температуры кристаллизации Т0 исследуемого образца и температуры кристаллизации 7 абсолютно чистого вещества. [25]
Вопросы теплопередачи имеют решающее значение при вулканизации толстостенных резиновых изделий. Наряду с экспериментальным определением температур в вулканизуемых изделиях при разработке тепловых режимов вулканизации в настоящее время находят широкое распространение расчеты температурных полей. Эффективность расчетов заметно возрастает в связи с освоением средств вычислительной техники. [26]
Теплота сгорания имеет важнейшее значение для оценки пожарной опасности веществ. Данные о теплоте сгорания используются при экспериментальном определении температуры самонагревания веществ, при расчете пределов воспламенения, группы горючести, температуры горения, удельной теплоты пожара и в других случаях. [27]
В практическом отношении расчет равновесия между жидкостью и паром при постоянном давлении предпочтительнее расчета при постоянной температуре, так как большинство процессов разделения смесей, основанных на использовании различия в летучестях компонентов, проводится при Р const. Нужно считаться также с тем, что экспериментальное определение температур кипения смесей при постоянном давлении проще, чем определение давлений паров при постоянной температуре. Метод расчета равновесия между жидкостью и паром по температурам кипения смесей особенно удобен, когда температуры кипения компонентов сильно различаются и возникают затруднения в использовании экспериментальных методов, основанных на аналитическом определении составов равновесных фаз. Прибегая к использованию этого метода, необходимо, однако, помнить о сделанных допущениях. Ясно, что основным условием, определяющим применимость этого метода, является небольшая теплота смешения. Очень важно не ошибиться сильно в ее оценке при отсутствии опытных данных. Некоторым ориентиром в этом отношении могут служить рассчитанные значения коэффициентов активности. Если они сравнительно невелики и больше единицы ( в случае, если стандартное состояние - чистый компонент), что свидетельствует о положительных отклонениях от идеального поведения, можно предполагать, что теплота смешения компонентов мала. Подобная оценка не годится для систем с отрицательными отклонениями от идеального поведения. [28]
Это является следствием двух причин. Одна из них состоит в том, что экспериментальное определение температуры замерзания легче, чем определение температуры кипения, так как температура кипения зависит в очень большой степени от давления. Однако, если для определения повышения температуры кипения пользоваться методом польского ученого Свентославского, то получаются достаточно хорошие результаты. Этот метод основан на непосредственном сравнении температуры кипения растворов и чистой жидкости. Вторая причина, которая касается обоих методов - криоскопи-ческого и, особенно, эбулиоекопического - состоит в том, что этими методами коэффициенты активности определяются непосредственно только для температур замерзания или кипения растворов. При этом измерение коэффициентов активности производится не при постоянной температуре, а при переменных температурах, так как величина 6 является функцией от концентрации. [29]
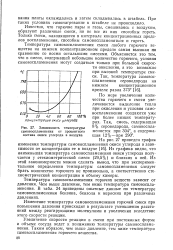 |
Зависимость температуры. [30] |
Страницы: 1 2 3