Зависимость - адсорбция
Cтраница 1
Зависимость адсорбции от количества изотопа-антиносителя ( разд. [1]
Зависимость адсорбции негидролизующихся радиоактивных изотопов от их концентрации можно выразить изотермой Ленг-мюра или Фрейндлиха. [2]
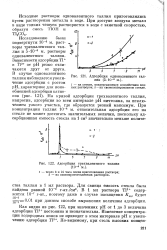 |
Адсорбция одновалентного таллия ( 5 - Ю-6 м..| Адсорбция трехвалентного таллия ( 10 - м.. [3] |
Зависимости адсорбции Т1 и Т18 от рН резко отличаются друг от друга. [4]
Зависимость адсорбции негидролизующихся радиоактивных изотопов от их концентрации можно выразить изотермой Ленг-мюра или Фрейндлиха. [5]
Зависимость адсорбции от концентрации уяснить нетрудно. Увеличение концентрации молекул адсорбтива в объеме увеличит и то их количество, которое оседает в единицу времени на поверхности адсорбента; следовательно, чем больше концентрация, тем больше адсорбция и наоборот. [6]
Зависимость адсорбции от концентрации при постоянной температуре может быть изображена графически; полученная таким образом кривая называется изотермой адсорбции. [7]
Зависимость адсорбции от концентрации примесей имеет сравнительно небольшое значение в количественном анализе. Химик обычно не имеет возможности сильно уменьшить концентрацию примесей, так как она обусловлена главным образом составом анализируемого объекта, а также методом анализа, который обычно приходится выбирать по другим соображениям. Большее значение имеет следующая особенность адсорбции. Адсорбция при образовании осадков зависит от характера находящихся в растворе ионов. Обычно раствор содержит различные ионы. Из них наиболее сильно адсорбируются те, которые дают с ионами осадка нерастворимые или малодиссоциирующие соединения. Таким сильно адсорбирующимся ионом является часто собственный ( одноименный) ион осадка, находящийся в данных условиях в избытке. [8]
Зависимость адсорбции от строения молекул адсорбата на графитированной саже позволяет разделять смесь нормальных и изосоединений: изобутана, - бутана, изопропилбензола, л-пропилбензола. Довольно большая разница между объемами удерживания нормального бутана и изобутана позволяет легко определять примеси изобутана в нормальном бутане. На графитированной саже также достаточно хорошо разделяются нормальные и вторичные спирты, благодаря различному строению их молекул. [9]
Зависимость адсорбции от потенциала проявляется при высокой адсорбируемости веществ. [10]
Зависимость адсорбции Г от равновесной концентрации с или равновесного парциального давления р при постоянной температуре называется изотермой адсорбции. Имеется несколько уравнений изотерм адсорбции, наиболее часто используются уравнения Лэнг м ю р а и Фрейндлиха. При выводе уравнения Лэнгмюра было сделано предположение, что поверхность адсорбента однородна и при максимальном заполнении образуется мономолекулярный слой. [11]
Зависимость адсорбции от концентрации адсорбата может иметь разную форму. [12]
Зависимость адсорбции из раствора на твердом теле от равновесной концентрации адсорбтива описывается обычной изотермой адсорбции. Для достаточно разбавленных растворов в этом случае пригодно эмпирическое уравнение Фрейндлиха или, что лучше - уравнение Ленгмюра. Теоретически применимо и уравнение Гиббса, но, так как поверхностное натяжение на границе твердое тело - раствор определить невозможно, то использовать это уравнение нельзя. [13]
Зависимость адсорбции от концентрации примесей имеет сравнительно небольшое значение в количественном анализе. Химик обычно не имеет возможности сильно уменьшить концентрацию примесей, так как она обусловлена главным образом составом анализируемого объекта, а также методом анализа, который обычно приходится выбирать по другим соображении. Большее значение имеет следующая особенность адсорбции. [14]
Зависимость адсорбции от температуры и вида га.а. Температурная зависимость газовой адсорбции сравнительно несложна. С повышением температуры, как правило, уменьшается количество адсорбированного газа при постоянном давлении, а при понижении температуры оно увеличивается. Отсюда, в со - ОТВететЖй Т Принципом смешений равновесий ( § ВТ), можно заключить, что адсорбция сопровождается выделением теплоты. [15]
Страницы: 1 2 3 4