Опыт - окисление
Cтраница 2
Преподаватель начинает занятие с демонстрации опыта окисления паров метилового спирта. Вначале кратко повторяют основные свойства метилового спирта. Преподаватель пишет на доске формулу спирта и говорит, что в данном опыте будет происходить окисление спирта; учащимся знакома реакция окисления - в простейшем варианте это присоединение кислорода. Преподаватель напоминает учащимся, что в метиловом спирте, согласно теории Бутлерова, все связи углерода насыщены и, казалось бы, кислороду присоединяться некуда. Однако опыт демонстрирует присоединение кислорода к спирту. В процессе проведения демонстрационного опыта остается время, и преподаватель может предложить учащимся продумать, каким образом происходит окисление спирта, и написать формулу конечного продукта. [16]
Описанные до сих пор в литературе опыты окисления кислородом углеводородов не дают, однако, ответов на поставленные вопросы вследствие чрезвычайно разнообразных экспериментальных условий, использованных различными авторами, а иногда и противоречивых результатов, полученных ими при окислении одного и того же углеводорода в сравнительно близких условиях опыта. [17]
Существование а-карбинольного десмотропа может быть доказано опытом окисления гидроокиси алкил-пиридиния. При этом образуется значительное количество соединения, содержащего СО-группу. [18]
К такому же выводу пришел М. И. Коновалов из опытов окисления псевдоку-мола и ксилилнитрометана ( см. стр. Автор предполагает, что ыитросоединение окисляется легче в момент своего образования. Предположение это ничего, очевидно, не объясняет. [19]
При отсутствии толуола совершенно аналогично может быть проведен опыт окисления ксилола. В этом случае образуется фта-левая кислота. [20]
Во избежание несчастных случаев можно заменить предложенный программой опыт окисления метилового спирта опытом окисления этилового спирта. [21]
Переносить на процессы дыхания данные, полученные в опытах окисления при высоких температурах и низких давлениях, нельзя уже по одному тому, что повышение внутренней температуры организма на какой-нибудь десяток градусов для него - вопрос жизни и смерти. [22]
 |
Кинетические кривые накопления перекисей при температуре 110. [23] |
В табл. 84 представлены данные по эффективности антиокислителей в опытах окисления двух образцов свиного жира, разной степени окисленности, и, кроме того, устойчивость этих жиров к окислению. [24]
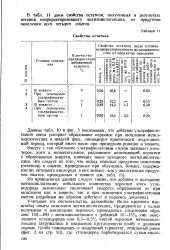 |
Свойства остатков. [25] |
Учитывая эти обстоятельства, дальнейшие ( более крупного масштаба) опыты окисления метилциклогексана, предпринятые с целью получения и накопления перекиси, проводились следующим образом: 150 - 180 г метилциклогексана с добавкой 10 - 15 % уже окисленного углеводорода или 0 3 - 0 5 % чистой перекиси метилциклогексана загружались в кварцевую круглодонную колбу с длинным горлом. Колба помещалась в воздушный термостат, описанный ранее ( фиг. [26]
Эти особенности, наблюдаемые при окислении смесей, подтверждаются и опытами окисления минеральных масел, представляющих собой широкую смесь углеводородов различного состава. [27]
С целью выявления влияния продолжительности реакции на выход продуктов были поставлены опыты постадийного окисления керогена сланца. Результаты одного из таких опытов - опыт 23а и 236 - при продолжительности окисления в первой стадии 8 ч и доокисления нерастворившихся в кислой среде веществ также 8ч показывают, что за 16ч реакции окислилось 96 6 % керогена сланца и было получено 21 4 % эфирного экстракта. Таким образом, при двухстадийном окислении время реакции может быть сокращено и скорость окисления увеличена. [28]
 |
Константы диссоциации окспферроцена. [29] |
Высказанные выше соображения о неустойчивовсти хиноидного состояния в молекуле ферроцена подкрепляются опытами окисления воздухом описанного ниже 1 1 -диоксиферроцена; при этом молекула разлагается с выделением неорганического соединения железа, образующийся циклопептадиснон изолирован в виде димера. [30]
Страницы: 1 2 3 4