Орби-таль
Cтраница 1
 |
Формы s - и р-орбиталей. [1] |
Орби-таль ( / 0) имеет шарообразную форму; электронная плотность в таких облаках является только функцией изменения радиуса. [2]
 |
Тригональные гибридные орбитали в этилене. [3] |
Орби-тали ( 180) и ( 181) имеют одинаковые по абсолютной величине коэффициенты, поскольку плоскость zz является плоскостью молекулярной симметрии. [4]
Орби-тали первых трех ( s, px и рй) перестраиваются и дают три sp2 - гибридных облака. Четвертый электрон ( рг) остается негибридным, его электронное облако в молекуле бензола не перерождается. [5]
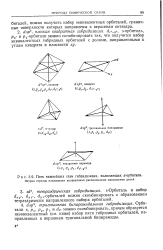 |
Пять важнейших схем гибридизации, включающих d - орбитали. [6] |
Орби-тали s, рх, ру, pz и dzi можно скомбинировать, причем образуется неэквивалентный ( см. ниже) набор пяти гибридных орбиталей, направленных к вершинам тригональной бипирамиды. [7]
 |
Схематическое расположение а-связей в молекуле этилена. [8] |
Орби-таль ( рис. 33) не обладает осевой симметрией, так как при вращении вокруг линии связи на 180 молекулярная орбиталь меняет знак на противоположный. [9]
Орби-тали, вовлеченные в супраповерхностные сдвиги, показанные на схемах ( 17) и ( 18), топологически аналогичны я-орбиталям цикло-пропенил-катиона - карбениевого иона, который в соответствии с обычными критериями Хюккеля является ароматическим. [10]
 |
Тригональные гибридные орбитали в этилене. [11] |
Орби-тали ( 180) и ( 181) имеют одинаковые по абсолютной величине коэффициенты, поскольку плоскость xz является плоскостью молекулярной симметрии. [12]
Поэтому орби-таль ( волновая функция) при переходе через узел меняет знак. [13]
Какие орби-тали используются для образования гибридных орбиталей связи атома иода. [14]
 |
Смешивание атомных р-орбиталей при образовании молекулярных. [15] |
Страницы: 1 2 3 4 5