Орби-таль
Cтраница 4
Образование ее из соответствующих атомных орби-талей сопровождается выделением энергии. Такую орбиталь называют связывающей. [46]
Комплексные соединения с октаэдрическими и квадратными орби-талями рассмотрены в гл. [47]
Полностью 3 / - орби-таль заполнена у цинка. Четвертый период заканчивается также благородным газом криптоном с полностью заполненной 4р6 - оболочкой. Эти металлы Sc - Zn образуют первую десятку элементов вставных декад. [48]
Ортогонализация атомной 28д - орби-тали не влияет на молекулярные орбитали или их энергии - она лишь меняет группировку термов в ЛКАО разложения. [49]
 |
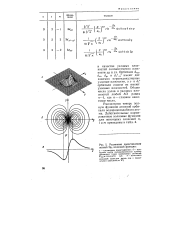
Орбитали dz2 и А2 - 2 в октаэдрическом поле лигандов. [50] |
Электроны, занимающие эти орби-тали ( их обозначают как е8 - орбитали), имеют большую энергию. На рис. 1.56 а показана схема расщепления энергетических уровней в октаэдрическом окружении иона-комплексообразователя. [51]
Так как s - орби-таль одинаково простирается во всех направлениях и имеет положительный знак, она одинаково взаимодействует со всеми а-орби-талями лигандов. Каждая из р-орбиталей металла может перекрываться только с 0-орбиталями двух лигандов, направленных вдоль определенной оси; знаки функций должны обеспечить сочетание орбита-лей. [52]
Обратные преобразования позволяют выразить гибридные орби-тали через атомные орбитали. [53]
В результате возникают четыре одинаковые гибридные орби-тали, которые направлены к вершинам тетраэдра. [54]
 |
Типы симметрии молекул ( ионов. [55] |
В первом случае гибридизация орби-талей приводит к образованию октаэдрической структуры, во втором-к образованию додекаэдрической структуры иона. В табл. 21.3 приведены типы симметрии и форм молекул ( ионов), отвечающих различным видам гибридизации. [56]
Поскольку один электрон на разрыхляющей орби-тали уничтожает связывающее действие электрона на связывающей орбитали, то молекула Не2 существовать не может. К такому же выводу приводит и метод валентных связей. [57]
Рассмотрим теперь полную функцию атомной орби-тали водородоподобного атома. [59]
Верхний индекс b обозначает связывающую орби-таль, а () - разрыхляющую. Для экваториальных лигандов более важным оказывается промотирование первого типа. [60]
Страницы: 1 2 3 4 5