Орбиталь - двойная связь
Cтраница 1
Орбиталь двойной связи и вакантная р-орбиталь катиона винильного типа оказываются во взаимно перпендикулярных плоскостях и перераспределение электронной плотности между ними осуществиться не может. Вместе с тем связь С - Hal в перечисленных выше соединениях имеет повышенную прочность из-за р-п сопряжения галогена с ненасыщенной группировкой ( или трехчленным кольцом), что также затрудняет диссоциацию соединения по этой связи. [1]
 |
Структура двуокиси углерода, основанная на коллинеар. [2] |
Кроме того, уменьшение взаимного отталкивания орбиталей двойных связей достигается их расположением в перпендикулярных плоскостях. При этом возникает приблизительно тетраэд-рическая конфигурация четырех электронных пар вокруг центрального атома углерода. [3]
Взаимодействие гг-орбиталей СН-связей с л - орбиталями двойной связи по механизму я, су-сопряжения, названного гиперконъюгацией, обозначается изогнутой стрелкой. Вследствие этого эффекта атомы водорода приобретают повышенную подвижность. Подобные соединения могут быть охарактеризованы как СН-кислоты. [4]
УФ: Необычное длинноволновое поглощение ясно указывает на некоторое перекрывание орбиталей двойных связей. [5]
Этот переход наблюдается в случае карбонильных соединений и заключается в переходе электронной пары п кислорода на разрыхляющую орбиталь двойной связи, которая при этом не разрывается, яо изменяет поляризацию. [6]
 |
Орбитальное соответствие для обменного взаимодействия синглет-ных карбенов с двойными связями.| Запрещенные взаимодействия триплетных карбенов с двойными. [7] |
Так как на каждой гибридной орбитали находится по одному электрону, они могут взаимодействовать и с занятой и с незанятой орбиталями двойной связи, так что полное число электронов при этом будет равно 3 и 1 соответственно. Оба эти типа взаимодействия примерно равноценны, и легко видеть, что они противоположны друг другу. В результате синхронная реакция запрещена. [8]
Тот факт, что соединение XXXI реагирует на 3 порядка быстрее, чем соединение XXX, указывает на более эффективное перекрывание вакантной р-орбитали с циклопропильными орбиталями, нежели с орбиталями двойной связи; этот факт согласуется и с теоретическими расчетами Хоффмана. [9]
Структура искаженной шестиугольной бипирамиды найдена для уранильных комплексов с бидентатными лигандами, например UO2 ( NO3) 3 - Возможно, что такая геометрия обусловлена группой UO, стремящейся принять линейную конфигурацию, и большим объемом орбиталей двойных связей на валентной оболочке атома урана по сравнению со связями с нитратными группами. [10]
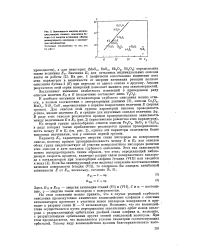 |
Зависимость энергии активации реакции полного окисления бу-тена-1 от энергии активации обмена молекулярного кислорода с кислородом катализатора. [11] |
На этом основании можно принять, что в случае реакций глубокого окисления промежуточное химическое взаимодействие олефинов с окисным катализатором протекает с участием ионов кислорода поверхности и приводит к разрыву связи М - О катализатора. Возможно, что это взаимодействие осуществляется путем перекрывания заполненных орбит ионов кислорода с разрыхляющими орбиталями двойной связи олефина и, возможно, с разрыхляющими орбиталями других связей окисляемой молекулы. При этом предполагается, что выполняется условие симметрии соответствующих орбиталей. [12]
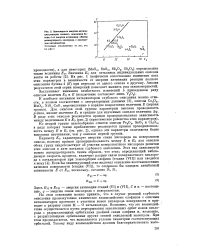 |
Зависимость энергии активации реакции полного окисления бу-тена-1 от энергии активации обмена молекулярного кислорода с кислородом катализатора. [13] |
На этом основании можно принять, что в случае реакций глубокого окисления промежуточное химическое взаимодействие олефинов с окисным катализатором протекает с участием ионов кислорода поверхности и приводит к разрыву связи М - О катализатора. Возможно, что это взаимодействие осуществляется путем перекрывания заполненных орбит ионов кислорода с разрыхляющими орбиталями двойной связи олефина и, возможно, с разрыхляющими орбиталями других связей окисляемой молекулы. При этом предполагается, что выполняется условие симметрии соответствующих орбиталей. [14]
В других случаях первой стадией процесса должно быть взаимодействие нуклеофила с молекулой субстрата. Как уже говорилось, низшей свободной орбиталью винильного субстрата обычно является разрыхляющая л - орбиталь двойной связи. Результатом взаимодействия нуклеофила с этой орбиталью является присоединение нуклеофила по двойной связи с образованием карбаниона. На второй стадии реакции происходит отщепление уходящей группы и, таким образом, происходит суммарное замещение уходящей группы на нуклеофил. Легко видеть, что такой процесс аналогичен реакциям производных карбоновых кислот, которые были нами рассмотрены в предыдущей главе. [15]
Страницы: 1 2