Орбиталь - неспаренный электрон
Cтраница 1
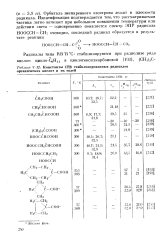 |
Константы СТВ стабилизированных радикалов органических кислот и их солей. [1] |
Орбиталь неспаренного электрона лежит в плоскости радикала. [2]
В я-радикалах орбиталь неспаренного электрона имеет р-ха-рактер и атом углерода находится в состоянии 5р2 - гибридизации; при переходе от молекулы к свободному радикалу происходит изменение гибридизации того атома, у которого возникает неспаренный электрон. [3]
F в орбиталь неспаренного электрона очень мал. Единственный возможный способ установления типа образующейся парамагнитной частицы состоит в сравнении экспериментального среднего значения - тензора, равного 1 9988, с теоретическими предсказаниями. Другие значения значительно ближе к чисто спиновому - фактору. [4]
В таких трифенилметильных бирадикалах орбиталью неспаренного электрона охватываются протоны двух фенильных и одной фениленовой группы аналогично тому, как это происходит в самом трифенилметиле. [5]
 |
Блок-схема спектрометра ЭПР. К - источник СВЧ излучения, В - волноводы, Р - объемный резонатор, Д - детектор СВЧ излучении, У - усилитель, М5 - электромагнит, П - регистрирующее устройство. [6] |
Эффект сверхсопряжения заключается в непосредственном перекрывании орбиталей неспаренного электрона и мага. В частности, в алкильных радикалах СТВ по этому механизму возникает на ядрах р-протонов. СТВ определяется конфигурационным взаимод. Эквивалентность СТВ с тремя протонами метильной группы в рассматриваемом случае обусловлена быстрым вращением группы СН3 относительно связи С - С. СТВ с Р - протонами определяется выражением ан В0 В2со826, где в - двугранный угол между 2рг - орби-талью а-утлеродного атома и связью СН, В04 - 1 ( Н Тл определяет вклад спиновой поляризации по ядерному остову ( конфигурационное взаимод. [7]
Химическая связь, образованная за счет взаимодействия орбиталей неспаренных электронов. [8]
В промежуточном случае и связь А - Ни орбиталь неспаренного электрона включают частично s - орбиталь атома А. Поскольку s - орбиталь имеет значительную отличную от нуля плотность вблизи ядра, когда один из связывающих электронов находится вблизи неспаренного электрона, их волновые функции будут иметь в некоторой степени характер s - функций. В силу этого оба рассматриваемых электрона стремятся расположить свои спины антипараллельно. Поскольку другой электрон связи А - Н ( находящийся у атома водорода) должен иметь спин, антипараллельный спину первого электрона, на протоне возникает результирующая положительная спиновая плотность. [9]
 |
Влияние магнитного поля на поляризацию Н хлороформа в реакции фотолиза дизопропилкетона в ССЦ. Сплошная кривая является результатом теоретического расчета. [10] |
Как известно, обменное взаимодействие в РП обусловлено перекрыванием орбиталей неспаренных электронов радикалов. [11]
 |
Константы СТВ ( в э и спиновые плотности в радикалах LIX и. [12] |
Расчеты по методу Мак-Лечлана показали, что в обоих радикалах орбиталь неспаренного электрона дважды вырождена. [13]
Другая причина, которая вызывает уширение линий, заключается в том, что орбиталь неспаренного электрона охватывает большое число магнитных ядер, но при этом не перекрывается с волновыми функциями других неспаренных электронов. Например, электрон, захваченный кристаллом фторида, может быть достаточно локализованным. Однако хвост его волновой функции может охватить несколько близлежащих элементарных ячеек. Подобное расщепление обычно не удается разрешить, но оно приводит к уширению линий. Принято называть такую линию уширенной негомогенно, хотя процесс, конечно, в данном случае не является релаксационным. [14]
 |
Спектр ЭПР ионов Мп2 в апатите. [15] |
Страницы: 1 2 3