Зависимость - потенциальная энергия
Cтраница 1
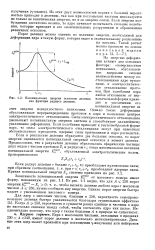 |
Потенциальная энергия осколков деления как функция радиуса деления. [1] |
Зависимость потенциальной энергии Е анс от массового номера имеет форму, показанную на рис. 1.1. Из рис. 1.1 видно, что для А С 250 порог энергии ЕрЯКС - E. А 250, нужно сообщать ему энергию. Однако порог энергии быстро падает с уменьшением массового номера. [2]
Зависимость потенциальной энергии от внешних параметров обусловливает собой появление внешних сил, с которыми данная система действует на окружающие тела или последние действуют на систему. [3]
 |
Зависимость энергии взаимодействия между ос-части-цей и атомным ядром. [4] |
Зависимость потенциальной энергии ядерного притяжения от расстояния г нам точно неизвестна, пока остается неизвестным закон действия ядерных сил. Однако потенциальная энергия ядерного взаимодействия ( притяжения), отрицательная по знаку, может быть принята постоянной по величине в ядре и резко возрастающей до нуля на его границе. С увеличением расстояния ядерные силы быстро убывают и на расстояниях, больших R, становятся практически равными нулю, здесь существуют только силы кулоновского отталкивания. [5]
График зависимости потенциальной энергии от некоторого аргумента называется потенциальной кривой. Анализ потенциальных кривых позволяет определить характер движения тела. [6]
График зависимости потенциальной энергии от некоторого аргумента называется потевцмлыюй кривой. Анализ потенциальных кривых позволяет определить характер движения тела. [7]
Кривая зависимости потенциальной энергии от деформационной координаты имеет вид, изображенный на фиг. Для квазилинейных молекул характерно, что центральный максимум не очень высок и что два минимума соответствуют сравнительно малым значениям деформационной координаты. [8]
График зависимости потенциальной энергии от некоторого аргумента называется потенциальной кривой. Анализ потенциальных кривых позволяет определить характер движении тела. [9]
График зависимости потенциальной энергии от сил деформации для ядерных колебаний очень похож на подобный график для деформации капли жидкости ( см. рис. 12), хотя в случае ядерных колебаний мы имеем более сложную систему взаимодействующих сил, описанных в этой главе ранее. [10]
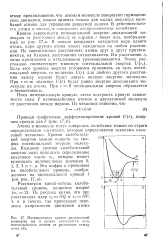
Диаграммы зависимости потенциальной энергии от координаты реакции часто применялись для рассмотрения типичных реакций ароматического замещения. На рис. 1 изображен профиль энергии для одной из них в том виде, в каком его использовал Меландер [91], чтобы воспроизвести ход реакций водородного обмена. Ветвь Л Б соответствует увеличению потенциальной энергии, вызванному первоначальной поляризацией ароматической системы при образовании я-комплекса и образованием реакционноспособной замещающей частицы из больших по объему реагентов. Как показано на этой диаграмме, реакция проходит через точку, отвечающую комплексу я но будет ли он в действительности реализоваться как промежуточное соединение, зависит от реакционной способности реагирующих веществ. В случае очень сильного электрофильного агента начальное повышение потенциальной энергии будет выражаться кривой А Б; в таком случае я-ком-плекс мог бы быть промежуточным соединением. По кривой ВГ начальная структура, подобная я-комплексу, превращается в а-комплекс с соответствующим повышением энергии вследствие потери энергии стабилизации ароматической системы. Кривая ДЕ соответствует комплексу о. Пересечение ВГ и ДЕ соответствует стадии, которая определяет скорость всей реакции, если, как показано на рисунке, образование а-комплекса лимитирует скорость реакции. С правой стороны графика эти изменения повторяются, а выигрыш в потенциальной энергии обусловлен исключительно выигрышем стабильности при образовании ароматической системы. [11]
 |
Потенциальная кривая двухатомной молекулы ( а и кривая зависимости силы взаимодействия атомов от расстояния между ними ( б. [12] |
Кривая зависимости потенциальной энергии двухатомной молекулы от расстояния между ее ядрами г имеет вид, изображенный на рис. 17 а. В начале координат находится ядро одного атома, ядро другого атома может находиться на любом расстоянии. На значительных расстояниях атомы друг к другу притягиваются, на близких расстояниях отталкиваются. На расстоянии ге силы притяжения и отталкивания уравновешиваются. [13]
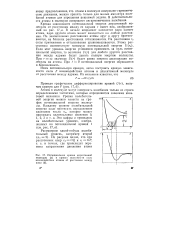 |
Потенциальная кривая двухатомной молекулы ( а и кривая зависимости силы взаимодействия атомов от расстояния между ними ( б. [14] |
Кривая зависимости потенциальной энергии двухатомной молекулы от расстояния между ее ядрами г имеет вид, изображенный на рис. 17, а. В начале координат находится ядро одного атома, ядро другого атома может находиться на любом расстоянии. На значительных расстояниях атомы друг к другу притягиваются, на близких расстояниях отталкиваются. На расстоянии ге силы притяжения и отталкивания уравновешиваются. [15]
Страницы: 1 2 3 4