Зависимость - потенциальная энергия - взаимодействие
Cтраница 1
Зависимость потенциальной энергии взаимодействия каждой пары валентно не связанных атомов от расстояния между ними, вообще говоря, можно представить в виде кривой. [1]
Зависимость потенциальной энергии взаимодействия двух молекул ипот ( г) от расстояния г между ними изображена на фиг. [2]
График зависимости потенциальной энергии взаимодействия молекул от расстояния между ними называют потенциальной кривой, участок ЛВС этой кривой принято называть потенциальной ямой, точку В - дном потенциальной ямы, а ординату DB - глубиной по-тенциальной ямы. [3]
Эта кривая передает зависимость потенциальной энергии W взаимодействия молекул от расстояния г между центрами молекул. По мере сближения молекул между ними возникает притяжение, кривая Щг) понижается. Легко видеть, что кривая Щг) имеет характерный минимум. [4]
Установим теперь примерный характер зависимости потенциальной энергии взаимодействия молекул Wn от г ( см) расстояния между ними. [5]
Установим теперь примерный характер зависимости потенциальной энергии взаимодействия молекул Wn от расстояния между ними. Дальнейшее сближение молекул возможно только за счет работы, совершаемой против сил Ът-талкивания. [6]
На рис. 3.1 схематически показана зависимость потенциальной энергии взаимодействия и ( г) между двумя молекулами от расстояния г между ними. [7]
На рис. 8.1 приведен график зависимости потенциальной энергии взаимодействия двух молекул от расстояния между ними. Пусть в точке г 0 находится молекула и вторая молекула приближается к ней из бесконечности. [8]
На рис. 163 дан график зависимости потенциальной энергии взаимодействия молекул от расстояния между ними. Расстояние гй соответствует минимуму потенциальной энергии, а следовательно, состоянию устойчивого равновесия. [9]
На рис. 1 - 1 изображена зависимость потенциальной энергии взаимодействия двух молекул от расстояния г между центрами молекул; сила, действующая на каждую из молекул, равна - ди / дг. [10]
В простейшем варианте теории рассматривается лишь зависимость потенциальной энергии взаимодействия молекул от конфигурации; во втором варианте теории, который, собственно, и относится к ассоциированным растворам, учитываются также изменения энтропии молекул при различных способах их контактирования и, тем самым, полуфеноменологически учитываются изменения сумм по внутренним состояниям молекул. [11]
 |
Термодинамическая поверхность идеального газа. [12] |
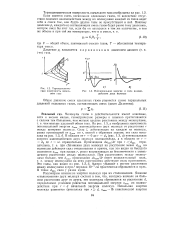
На рис. 1.3, а изображена зависимость потенциальной энергии итт взаимодействия двух молекул от расстояния г между центрами молекул. В области от г 0 до г d0 ( рис. 1.3, а) потенциальная энергия взаимодействия двух молекул положительна, а в области от г d0 до г оо отрицательна. Эти силы, как видно из рис. 1.3, б, быстро убывают с ростом расстояния между молекулами и при г порядка 10 7 см практически обращаются в нуль. [13]
В простейшем варианте теории рассматривается лишь зависимость потенциальной энергии взаимодействия молекул от конфигурации; во втором варианте теории, который, собственно, и относится к ассо-растворам, учитываются также изменения энтропии мо-при различных способах их контактирования и тем самым полуфеноменологически учитываются изменения сумм по внутренним состояниям молекул. [14]
 |
Зависимость потенциальной энергии и силы взаимодействия двух молекул от расстояния между центрами молекул. [15] |
Страницы: 1 2