Зависимость - потенциальная энергия - взаимодействие
Cтраница 2
На рис. 1.3, а изображена зависимость потенциальной энергии ип взаимодействия двух молекул от расстояния г между центрами молекул; сила ( рис. 1.3, б), действующая на каждую из молекул, равна производной от ип по г, взятой с обратным знаком. В области от г 0 до г - d0 потенциальная энергия взаимодействия двух молекул положительна, а в области от г d0 до г оо отрицательна. Эти силы быстро убывают с ростом расстояния между молекулами и при г порядка 10 - 7 см практически обращаются в нуль. В точке г dmm сила взаимодействия молекул равна нулю. [16]
Характер действия межмолекулярных сил в первую очередь обусловлен зависимостью потенциальной энергии взаимодействия частиц от расстояния г между ними. [17]
На рис. 171 дан, кроме того, график зависимости потенциальной энергии взаимодействия молекул от расстояния между ними. [18]
На рис. 17 представлена группа кривых ( по вычислениям Фервея и Овербека), показывающих зависимость потенциальной энергии взаимодействия двух коллоидных частиц от расстояния между ними; взяты наиболее вероятные значения потенциала поверхности и ван-дер-ваальсового притяжения. При повышении концентрации электролита, что соответствует увеличению значений к, отталкивание постепенно переходит в притяжение при достаточно малых расстояниях между частицами. [19]
На рис. 8.3 совмещены два рисунка: 1) зависимость результирующей силы F и 2) зависимость потенциальной энергии взаимодействия ф от расстояния между частицами. [20]
Автор: Взаимодействие двух молекул можно качественно описать с помощью кривой, изображенной на рис. 23.1. Эта кривая передает зависимость потенциальной энергии W взаимодействия молекул от расстояния г между центрами молекул. По мере сближения молекул между ними возникает притяжение, кривая W ( r) понижается. Легко видеть, что кривая W ( г) имеет характерный минимум. [21]
Отмеченное отличие поведения реального газа от идеального обусловлено наличием сил взаимодействия между молекулами, которые не учитываются в модели идеального газа. Зависимость потенциальной энергии взаимодействия молекул и от расстояния г между ними показана на рис. 7.2. Характер зависимости ыя / ( г) можно предсказать на основании самых общих наблюдений. Так, тот факт, что газы конденсируются, свидетельствует о существовании сил притяжения на больших расстояниях между молекулами, а очень сильное сопротивление жидкостей сжатию говорит о том, что на малых расстояниях между молекулами действуют силы отталкивания. При низких плотностях газа ( р - - 0) расстояние между молекулами значительно ( г 0) и силы притяжения малы ( рис. 7.2), а поэтому свойства реальных газов близки к идеальным. [22]
Выясним природу теплового расширения. Для этого вновь рассмотрим зависимость потенциальной энергии взаимодействия частиц от расстояния. [23]
Сначала рассмотрим энергию колебаний атомов в молекуле. На рис. 9.5 качественно показана зависимость потенциальной энергии взаимодействия атомов, образующих молекулу. [24]
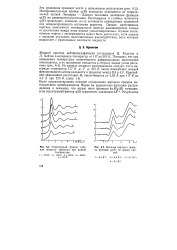 |
Структурный фактор a ( S для жидкого криптона при разной.| Влияние верхнего g ( R на вой. [25] |
Экспериментальные кривые ф () несколько отличаются от теоретической кривой Леннарда - Джонса числовым значением ( f ( R) на равновесном расстоянии. Расхождение в глубине ( f ( R) происходит, очевидно, из-за неточности приведенных уравнений конденсированного состояния вещества. Однако качественная зависимости потенциальной энергии взаимодействия атомов от расстояния между ними вполне удовлетворительна. Лучшее согласование теории с экспериментом может быть достигнуто, если наряду с парными учитывать многочастичные взаимодействия, роль которых возрастает с увеличением плотности жидкости. [26]
Страницы: 1 2