Зависимость - активность
Cтраница 1
Зависимость активности от степени обмена изучена нами на декатионированных, кальциевых, кальций-дека-тионированных и лантан-декатионированных формах. [1]
Зависимость активности от удельной поверхности катализатора 5УД размеры его зерен da и эквивалентного радиуса пор ru p зерне катализатора следует рассматривать в совокупности. [2]
Зависимость активности от концентрации Pd дает кривую с 3 паками с максимальным различием в активности в 2 раза ( активность отнесена к 1 г Pd) и в 3 5 при отнесении активности к 1 г катализатора. Неясно, являются ли эти различия реальными или они обусловлены неучетом истинной поверхности Pd. Полученные результаты интерпретированы по теории ансамблей в предположении, что активный центр состоит из 4 атомов Pd, а лимитирующей стадией реакции является прямой перенос Н2 между двумя молекулами циклогексена. [3]
Зависимость активности кат - pa и энергии активации от % - ного содержания Re в кат-ре. [4]
Зависимость активности ( коэффициента активности у) от концентрации Ci для многокомпонентных растворов не является однозначной. [5]
Зависимость активности от таких дефектов, как вакантные места, трещины, дислокации, ребра между гранями, в настоящее время еще не определена, но активность должна быть, по-видимому, различна для отдельных твердых веществ и типов каталитических реакций. [6]
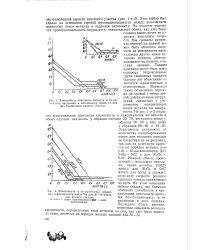 |
Зависимость константы скорости а от количества введенных в катализатор ионов Li для А1 - Si-образцов разного состава. [7] |
Зависимость активности от количества адсорбированных ионов для исходных окислов не представлена на рисунках, так как их константы скорости на порядок меньше, чем у А1 - Si-катализаторов. Ионный обмен, проведенный с исходными окислами, также невелик ( 0 025 мэкв / г для А12О3 и 0 07 мэкв / г для SiO2) и снижает константу скорости реакции крекинга кумола практически до нуля. На этом основании можно сказать, что большая обменная способность и крекирующая активность присуща А1 - Si-комплексу, а не входящим в него окислам. [8]
Зависимость активности g от концентрации примеси z изображена на рис. 7 ( ср. [9]
Зависимость активности ионов Н от активности ионов ОН - и рН от рОН видна из следующей таблицы. [10]
Зависимость активности ионов в обменнике от его набухаемости, определяемой степенью затвердевания, вытекает из новых работ Гюнтер ( диссертация, Лейпциг, 1951 г., у Штауде), в которых был изучен обмен солей серебра с некоторыми суль-фокислотными смолами конденсационного типа в Н - форме. Равновесные концентрации ионов определялись как известными аналитическими методами, так и потенциометрически. [11]
 |
Характер восстановления активности адсорбента при регенерациях. [12] |
Зависимость активности адсорбента а ( по отношению к первоначальной его активности а0) от числа регенераций N представлена на рис. VIII-3. Приведенная кривая показывает, что наибольшее снижение активности адсорбента наблюдается после первой регенерации. В дальнейшем активность снижается постепенно и в меньшей степени. Такой характер восстановления активности адсорбента объясняется тем, что при регенерации часть его активной поверхности остается занятой адсорбированными компонентами и в дальнейшем исключается из участия в процессе адсорбции. [13]
Зависимость активности низкопроцентных катализаторов по отношению к дегидрогенизации и СБ - дегидроциклизации от температуры восстановления платины. Катализаторы, содержавшие 3 - 4 % платины, готовили в количестве 20 мл. [14]
Никакой зависимости активности уропепсина от количества собраний за сутки мочи не установлено. [15]
Страницы: 1 2 3 4