Бифторид - аммоний
Cтраница 2
Трифторид азота получается электролизом расплава бифторида аммония или фторированием азотсодержащих органич. Термодинамически возможен синтез из элементов в разряде. Применяют в производстве тетрафторгидразина, для сварки металлов при горении смеси NF3 с водородом. [16]
Метод Руффа заключается в электролизе расплавленного безводного бифторида аммония, который проводится в обогреваемом медном электролизере с медным катодом и угольным анодом. Газ, получаемый в результате электролиза, кроме трех-фтористого азота содержит озон, кислород, закись азота, водород, азот и фтористый водород. По сообщениям Саймонса 10и, трехфтористый азот является продуктом электролиза растворов пиридина, пиперидина и анилина во фтористом водороде. [17]
Реакция разложения с образованием тетрафторгидразина и бифторида аммония, экспериментально доказанная Лоутоном и Вебером [137], медленно протекает уже при комнатных температурах. При повышении температуры реакция ускоряется. [18]
Определение фосфора в белой саже и бифториде аммония, Отч. [19]
Получаемые из отходящих фтористых газов фторид и бифторид аммония могут служить полупродуктами и для производства концентрированного фтористого водорода. [20]
Окситрифторид азота реагирует с аммиаком, образуя бифторид аммония. [21]
Трифторид азота может быть синтезирован путем электролиза бифторида аммония и путем фторирования ряда [ неорганических и органических веществ. Он синтезируется также из азота и фтора в разряде или при каком-либо ином инициировании процесса. [22]
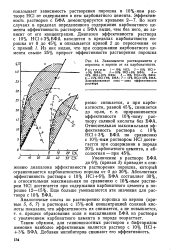 |
Зависимости растворимости q порошка и кернов от их карбонатности. [23] |
Таким образом, для глинокислотных растворов с бифторидом аммония наиболее эффективным является раствор с 10 % НС1 3 % БФА. Добавки ингибиторов снижают его эффективность. [24]
Проверка лабораторных регламентов по получению фтористого водорода, бифторида аммония и белой сажи, Отч. [25]
Имеющиеся данные позволяют рекомендовать обработку пластов с применением бифторида аммония. [26]
Результаты исследований подтверждают, что наиболее эффективной концентрацией бифторида аммония во всех вариантах исследований является 3 %, а с увеличением его добавки растворимость резко ухудшается. При высоких концентрациях бифторида аммония ( свыше 15 %) происходит образование геля в виде студенообразной массы и выпадение БФА из раствора в осадок. [27]
Установлено экспериментально, что иодометрическое определение кислотности в образцах бифторида аммония дает заниженные результаты. [28]
Различные модификации электролитического процесса заключаются главным образом в замене бифторида аммония другими соединениями азота. Так, описан электролиз раствора пиридина в безводном фтористом водороде. [29]
Кольбарн и Джонсон [29] установили, что при электролизе бифторида аммония образуются Дифтордиазины в качестве побочных продуктов. Выход дифтордиазинов составляет 5 - 10 % от количества газа, сконденсированного в ловушке при - 196 С. Выходы фторидов азота малы, практического интереса метод не представляет. [30]
Страницы: 1 2 3 4