Кривая зависимость - растворимость
Cтраница 1
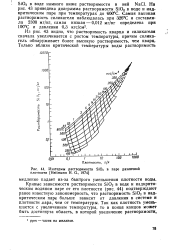 |
Изотермы растворимости SiO2 в паре различной плотности [ Heitmann H. G., 1974 ]. [1] |
Кривые зависимости растворимости SiO2 в воде и надкритическом водяном паре от его плотности ( рис. 44) подтверждают ранее известную закономерность, что растворимость SiO2 в надкритическом паре больше зависит от давления в системе и плотности лара, чем от температуры. [2]
В соответствии с этим кривые зависимости растворимости компонентов системы от температуры, имеют весьма различающийся для различных систем вид, и это оказывает серьезное влияние на ход процессов перегонки и конденсации систем частично растворимых компонентов ( см. стр. [3]
На рис. 29 приведены кривые зависимости растворимости различных кристаллогидратов сульфата церия от температуры. Этой зависимостью пользуются для переведения в раствор сульфатных продуктов при разложении руд, содержащих церий, торий и лантаниды. [4]
Вместе с тем наклон кривой зависимости растворимости полимера от соотношения количеств растворителя и осадителя не должен быть слишком крутым, иначе частицы всех молекулярных весов будут осаждены при добавлении очень малого количества осадителя, что сильно затруднит контроль за величиной фракций. В таких случаях фазовое равновесие очень легко нарушается в результате испарения или других случайных потерь растворителя или осадителя. Выбор системы растворитель - осадитель очень удобно осуществить, пользуясь кривой турбидиметрического титрования ( стр. Если для данной системы наблюдается резкое возрастание мутности при добавлении малого количества осадителя, то проводить фракционирование будет затруднительно. Если же мутность повышается вначале слабо, а затем очень резко, то это указывает на процесс агрегации [17, 18], и в таких системах при осаждении может не происходить разделения по молекулярным весам. [5]
Эти кривые можно рассматривать как кривые зависимости растворимости от температуры для каждого чистого компонента в растворе. Если принятые выше допущения справедливы, по таким кривым можно вычислить значение ЛЯ. И наоборот, если значение АН известно, можно рассчитать эти кривые. [6]
Эти кривые можно рассматривать как кривые зависимости растворимости от температуры для каждого чистого компонента в растворе. Если принятые выше допущения справедливы, по таким кривым можно вычислить значение АЯ. И наоборот, если значение АЯ известно, можно рассчитать эти кривые. [7]
Для жидкостей, частично растворимых одна в другой, характерны параболические кривые зависимости растворимости от температуры. Каждая из кривых состоит из двух ветвей, сходящихся вместе в температурной точке К ( рис. 3.5) наибольшей растворимости. [8]
 |
Пикнометры. Гей-Люссака ( а, ж, Менделеева ( б, Оствальда ( в, обычный ( г, U-образный ( д, Рейшауэра ( е и с - плоской пришлифованной крышкой ( л. [9] |
Гей-Люссак Жозеф Луи ( 1778 - 1850) - французский химик, открыл один из газовых законов, впервые ( 1819 г.) построил кривые зависимости растворимости солей в воде от температуры. [10]
Следует отметить неприменимость уравнения Генри для определения растворимости газа в силу зависимости константы Генри ( Г) от давления, а также значение объемных эффектов растворения, характеризуемых величиной парциального мольного объема газа, и сложный вид кривой зависимости растворимости, характеризуемой мольной долей растворенного газа а 2, от давления. [11]
По диаграмме взаимной растворимости двух жидкостей определить: 1) до какой температуры надо охладить раствор, содержащий 40 % фенола, чтобы выделился фенол; 2) состав фаз 50 % раствора при температуре 50; 3) состав фаз в заданной точке под кривой ЕВ С; 4) указать ва графике кривые зависимости растворимости фенола в воде и воды в феноле от температуры; 5) указать на графике области насыщенных и ненасыщенных растворов. [12]
Наличие перегибов на кривых зависимости растворимости от температуры указывает на взаимодействие растворенных веществ с растворителями, даже с такими инертными, как бензол, ацетон или этиловый спирт. Однако в гексанеэти эффекты не наблюдаются. Мартин и Пинк [167] изучали растворимость цинковых мыл жирных кислот в ряде органических растворителей и установили, что и в этом случае кривые зависимости растворимости от температуры имеют ту же форму-с характерным резким повышением растворимости при некоторой критической температуре растворения. [13]
Однако, начиная с некоторой температуры, наблюдается слабая зависимость растворимости от температуры. Концентрации, отвечающие излому на кривых зависимости растворимости от температуры, приблизительно соответствуют концентрациям центров сорбции, найденным независимым путем. При температурах, близких к температуре плавления полипропилена, наблюдается быстрое увеличение растворимости. [15]
Страницы: 1 2