Кривая зависимость - растворимость
Cтраница 2
Изменение температуры влияет не только на растворимость, но, нередко, и на состав осадков, особенно, если осадок является кристаллогидратом: Повышение температуры образования осадка обычно приводит к уменьшению числа молекул воды в кристаллогидрате. Такого рода процессы вызывают резкие изломы на кривой зависимости растворимости от температуры. [16]
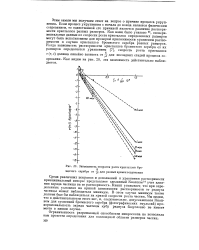 |
Зависимость скорости роста кристаллов бромистого серебра от - для разных времен созревания. [17] |
Среди различных поправок и дополнений к уравнению растворимости принципиальный интерес представляет сделанный Кнаппом18 учет влияния заряда частицы на ее растворимость. Кнапп указывает, что при определенных условиях на кривой зависимости растворимости от радиуса частицы может наблюдаться минимум. В-этом случае минимум также должен был бы наблюдаться на кривой скорости роста частиц. Мы видим, что в действительности этого нет, и, следовательно, допускавшаяся Кнаппом для суспензий бромистого серебра ( фотографических эмульсий) пропорциональность заряда частицы кубу радиуса безусловно не имееет места в нашем случае. [18]
Другим видом взаимодействия фаз в хроматографической системе при высоких давлениях является растворение неподвижной жидкости в элюенте. Термодинамическое рассмотрение процесса растворения жидкостей и твердых тел в сжатых газах приведено, например, в работе [7], где дается термодинамическое объяснение формы кривой зависимости растворимости конденсированной фазы в газе от давления, а также указывается, что теоретический количественный расчет растворимости веществ в сжатых газах весьма труден вследствие сложности поведения газовых растворов при высоких давлениях. Следует отметить, что величина растворимости может быть весьма значительной. Так, например, азот при 100 С и 1000 атм растворяет до 10 мол. Большие количества жидких углеводородов растворяются в газе, находящемся в соприкосновении с нефтью на больших глубинах. Механизм растворения веществ в сжатых газах связан с межмолекулярными взаимодействиями и принципиально не отличается от механизма растворения в жидкости. Однако в силу того, что плотность газового раствора зависит от давления сильнее, чем плотность жидкости, картина межмолекулярных взаимодействий в газовом растворе значительно сложнее, чем в жидком. [19]
Различные соли лития играют большую роль в процессе переработки литийсодержащего сырья и в аналитической химии лития. Такое различие в растворимости солей позволяет отделять литий от других щелочных металлов, вместе с которыми он-обычно встречается в природе. На рис. 61 изображены кривые зависимости растворимости карбоната и сульфата лития от температуры, причем для сравнения приведена кривая растворимости сульфата калия. Кривая растворимости - карбоната калия выходит за пределы масштаба, принятого на рис. 61, как это легко видеть, сопоставляя приводимые ниже цифры. [20]
 |
Кинетика растворения 4 4 - ДДТ в веретенном масле. [21] |
В этой же таблице приведены значения растворимости технического ДДТ, вычисленные по данным растворимости 4 4 - ДДТ, полученным при различных температурах. Данные по растворимости 4 4 - ДДТ при различных температурах графически изображены на рисунке. Рассматривая данные табл. 8 и кривые зависимости растворимости 4 4 - ДДТ от температуры, мы приходим к следующим выводам. [22]
Изменение температуры влияет не только на растворимость, но, нередко, и на состав осадков, особенно, если осадок является кристаллогидратом. Повышение температуры образования осадка обычно приводит к уменьшению числа молекул воды в кристаллогидрате. Такого рода процессы вызывают резкие изломы на кривой зависимости растворимости от температуры. [23]
Далее следует отметить, что при уточнении уравнения Оствальда - Фрейндлиха указывалось на один очень серьезный недостаток этого уравнения, заключающийся в следующем. Предполагается непрерывное увеличение растворимости с уменьшением размера частиц. Для устранения этого недостатка Кнапп [184] предположил, что частицы несут небольшой поверхностный заряд, так что общая поверхностная энергия представляет собой сумму нормальной поверхностной и электрической энергий. На основании таких предположений он вывел для изолированных заряженных сфер уравнение, которое на кривой зависимости растворимости от размера кристалла дает максимум. [24]
Наличие перегибов на кривых зависимости растворимости от температуры указывает на взаимодействие растворенных веществ с растворителями, даже с такими инертными, как бензол, ацетон или этиловый спирт. Однако в гексанеэти эффекты не наблюдаются. Мартин и Пинк [167] изучали растворимость цинковых мыл жирных кислот в ряде органических растворителей и установили, что и в этом случае кривые зависимости растворимости от температуры имеют ту же форму-с характерным резким повышением растворимости при некоторой критической температуре растворения. [25]
Страницы: 1 2