Ортосиликат - магний
Cтраница 1
Ортосиликат магния встречается в природе в виде минерала форстерита и может быть получен искусственным путем. [1]
Ортосиликат магния Mg2SiO4, соответствующий минералу форстериту, также получается искусственным путем. Это тугоплавкое соединение ( л1890 С), является изолятором ( f 10 - 16 - ICH7 См / м), существует только в виде одной кристаллической модификации. [2]
Для ортосиликата магния ( форстерита) характерна островная структура - кремпекислородпые тетраэдры соединяются между собой через ионы Mg2, образующие с окружающими кислородами неправильные окта-эдрические группы ( MgOe), т.е. каждый ион магния окружен 6 ионами кислорода, а каждый ион кислорода, в свою очередь, координируется с 3 ионами магния. [3]
Подтверждением этому может служить успешное применение дунита - ортосиликата магния в качестве магниевого удобрения на кислых почвах. Переходу магния из дунита в почвенный раствор способствует и кислая реакция. [4]
Оксиды железа, поглощаемые огнеупором из плавильной пыли, разрушают высокоогнеупорный ортосиликат магния, образуя при взаимодействии с Fe2O3 легкоплавкий фаялит, вытекающий из кирпича с образованием каверн. Одновременно возникают легкоплавкие эвтектики с температурой плавления примерно 1300 С. Образовавшиеся расплавы мигрируют из наиболее нагретой рабочей зоны огнеупора до температурных границ застывания соответствующих расплавов. [5]
В свете этого положения мы можем утверждать, что размеры полостей ортосиликатов магния, цинка и кадмия, а также моносиликатов, исключают возможность проникновения внутрь их воды. [6]
Одновременно с указанными выше реакциями избыток MgO соединяется со свободной SiO2 в ортосиликат магния, а с полуторными окислами - в шпинелиды. [7]
Химического взаимодействия форстеритового кирпича с реагирующей массой не наблюдается, что объясняется химической стойкостью ортосиликата магния и пе-риклаза к действию сульфата натрия и Na2O при 1000 С. [8]
 |
Характеристика фазовых равновесий системы MgO - Si02. [9] |
Компоненты MgO и SiO2, вступая между собой в химическую реакцию, образуют два соединения: ортосиликат магния 2MgO - SiO2, или форстерит, который плавится без разложения, и метасиликат магния MgO - SiO2, или энстатит, плавящийся с разложением. [10]
Муллит и кварц, составляющие основу кристаллической фазы высоковольтного фарфора, термодинамически более стабильны, чем мета - и ортосиликат магния, слагающие стеатитовую и форстеритовую керамику. Вероятно, и полевошпатовая стекловидная фаза в фарфоре более устойчива в сравнении со стекловидной фазой в стеатитовых и форстеритовых материалах. [11]
Оболочка литосферы, содержащая кислые породы ( например, ме-тасиликат кальция CaSiO3), имеет глубину 100 км от поверхности Земли, а основные породы ( например, ортосиликат магния Mg2SiO4) залегают до глубины 1200 км. Кислая оболочка литосферы состоит главным образом из гранитов и сланцев. Основная оболочка литосферы содержит оливин и другие родственные ему минералы. [12]
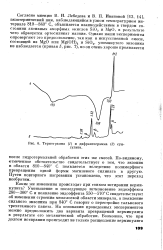 |
Термограмма ( 1 и дифрактограмма ( 2 сун-гулита. [13] |
Согласно мнению В. И. Лебедева и В. П. Ивановой [13, 14], экзотермический пик, наблюдающийся в узком температурном интервале 810 - 840 С, объясняется взаимодействием в твердом состоянии активных аморфных окислов Si02 и MgO, в результате чего образуется ортосиликат магния. [14]
К группе силикатов магния с обособленными изолированными тетраэдрами относится минерал оливин ( Mg, Fe) 2 [ SiOJ. Характерно для них то, что в ортосиликате магния некоторые ионы магния можно заменить двухвалентным железом. [15]
Страницы: 1 2