Температурная зависимость - реакция
Cтраница 1
 |
Зависимость стационарной ско - 2 4-рости реаццип для механизма ( X от температуры. [1] |
Температурные зависимости реакций, входящих в детальный механизм, часто сильно различаются. Энергия активации взаимодействия веществ AZ и BZ занимает промежуточное положение между энергиями активации адсорбции и десорбции E3 - tQ - 150 кДж / моль. Квазистационарный периодический режим будет, в частности, выгоден в тех областях изменения температуры Т Т Т2, где кинетические зависимости от этого параметра вогнутые. [2]
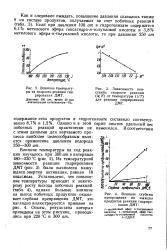
Из температурной зависимости реакции гидрирования ДМТ ( рис. 3) была вычислена кажущаяся энергия активации, равная 18 ккал / моль. [4]
Аналогично исследовалась температурная зависимость реакции метана. При температуре 300 С водород и окись углерода реагируют целиком. В условиях, когда ранее рассмотренные реакции уже полностью завершились, реакция с метаном только начинает проходить в заметной мере. [5]
 |
Зависимость скорости.| Зависимость скорости взаимодействия K [ PtPyCl3 ] с этиламином от концентрации K [ PtPyCl3 ]. [6] |
Было проведено изучение температурной зависимости реакций K [ PtPyCl3l с метил - и этиламином. [7]
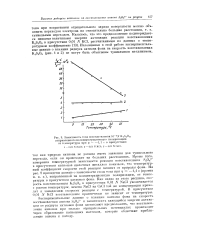 |
Зависимость тока восстановления 10 3N KaSaOg, исправленного на концентрационную поляризацию от температуры при р - - 1 1 в присутствии. [8] |
Кроме того измерения температурной зависимости реакции восстановления S2082 - в присутствии катионов щелочных металлом показали, что температурный коэффициент скорости этой реакции зависит от природы фона. Как видно из этого рисунка, скорость восстановления K2S208 в присутствии 0 01 N NaCl увеличивается с ростом температуры; замена NaCl на CsCl той же концентрации приводит к замедлению скорости реакции с температурой. Экспериментальные данные о влиянии катиона фона на скорость восстановления аниона S2082 и зависимость кажущейся энергии активации от радиуса катионов фона заставляют предположить, что восстановление анионов при сильно отрицательных потенциалах происходит через образование катиошшх мостиков, которые облегчают приближение аниона к катоду. [9]
В этом случае для корректной обработки температурной зависимости реакции необходимо учитывать теплоты ионизации ионогенных групп субстрата или активного центра фермента. [10]
При температурах 500 С реакция становится обратимой ( температурная зависимость реакции основание - антиоснование. [11]
Как видно из рис. 7.20 и 7.21, температурная зависимость реакции выражена крайне слабо. [12]
Первый из использованных образцов графита представлял собой стержень спектрографического графита длиной 50 мм и диаметром 6 2 мм. Экспериментальные данные для температурной зависимости реакции при давлении водяного пара 22 мкм рт. ст. приведены на фиг. Экспериментальные точки представлены зачерненными кружками. Прирост давления со скоростью 1 10 - 3 мм рт. ст. / мин соответствует реагированию 0 92 - 1015 молекул углерода в секунду. [13]
Общая кинетика реакции определяется во многих случаях скоростями диффузии реагента. Это может быть установлено путем измерения температурной зависимости реакции. Если энергия активации равна нескольким килокалориям на моль, ход реакции обусловлен диффузионными процессами, поскольку энергия активации большинства химических реакпий составляет не единицы, а десятки килокалорий на моль. [14]
Таки образом, является очевидным, что главная часть реакции при таких низких температурах идет на стенке, действующей как катализатор. Температурная зависимость таких гетерогенных реакций часто оказывается совсем иной, нежели температурная зависимость ооычных реакций, протекающих в газовой фазе. Причиной ьтого можно считать уменьшение концентрации реагентов на поверхности, перевешивающее возрастание скорости реакции, обусловленное температурой. Хотя подобных опытов и не производилось, представляется вероятным, что при низких температурах окисление формальдегида становится преимущественно гетерогенной реакцией; окисление же ацетальдегида становится цепной реакцией при высоких температурах. [15]
Страницы: 1 2