Температурная зависимость - скорость
Cтраница 2
Температурная зависимость скорости образования свободного серебра выражается для всех образцов желатины параллельными прямыми, что указывает на одинаковую энергию активации восстановительного процесса, независимо от природы желатины. [16]
Температурная зависимость скорости процессов изменения светочувствительности и роста вуали также подчиняется уравнению Аррениуса, причем для первого образца желатины соответствующие прямые оказываются параллельными прямой для свободного серебра. [17]
Температурная зависимость скоростей простых химических реакций выражается законом А. [18]
Изучена температурная зависимость скорости пирогидролиза фторида алюминия в области температур 400 - 600 С. Величина энергии активации, вычисленная по полученным данным, составляет 89 0 кдж / моль. [19]
Исследование температурной зависимости скорости кристаллизации показало, что для смесей полимеров в широком диапазоне их соотношений сохраняются два максимума скорости кристаллизации, совпадающие ( с точностью до Г) с температурами максимальной скорости кристаллизации дивинилового ( Т - 55 С) и изопренового ( Т - - 25 С) каучуков. При температуре Т - 55 С полиизопрен практически не кристаллизуется и закономерности кристаллизации не отличаются от тех, которые наблюдаются для смесей дивинилового каучука с некристаллизующимися. То же происходит при Т - 25 С, где при малом содержании дивинилового каучука его можно рассматривать как некристаллизующийся. Независимая кристаллизация этих двух каучуков в смеси подтверждается ж характером плавления. [20]
 |
Значения k. и Г. [21] |
Из температурной зависимости скорости переноса авторы определили энергию активации процесса, которая для метана и аргона оказалась соответственно равной Е 4790 и 3820 кал / молъ. Изостерические теплоты адсорбции для метана и аргона соответственно равны Д 5900 и 4910 кал / молъ. [22]
Из температурной зависимости скорости травления, представленной в координатах lg со от обратной температуры, можно видеть, что при некоторых значениях температуры имеется переход, соответствующий изменению кинетического механизма реакции на диффузионный. [23]
Изучение температурной зависимости скорости окисления ( энергии активации) часто позволяет определить механизм окисления и изменения его при изменении температуры. На практике возможны заметные отступления от указанных более простых законов окисления. [24]
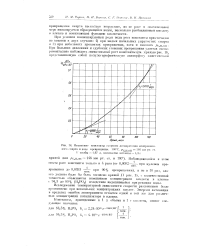 |
Изменение константы спорости дегидратации изопропило. [25] |
Исследование температурной зависимости скорости разложения было произведено при нескольких концентрациях кислот. Энергия активации в пределах ошибок эксперимента остается одной и тон же для различных концентраций катализатора в пленке. [26]
Сопоставление температурных зависимостей скорости термического окисления и накопления а-моноклинной структуры в исследованных полиамидных пленках позволяет сделать вывод о том, что изменение механических свойств при хранении может обуславливаться и структурными превращениями. [27]
 |
Зависимость lg kz f ( 1 / Г для окисления меди в кислороде. [28] |
График температурной зависимости скорости химической коррозии металла ( см. рис. 82, б) удобен для нахождения отсутствующих значений скорости при каких-либо интересующих нас температурах. Он же может быть использован для определения постоянных Л и Q уравнений ( 242) и ( 243) из опытных данных. Поэтому для определения значений постоянных уравнения ( 243) опытные данные охватывают прямой у - а Ьх методом наименьших квадратов. [29]
Изучая температурную зависимость скорости мономолекулярной реакции, можно установить кинетические константы этой реакции: энергию активации Е, предэкспоненциальный множитель В и период полураспада, дающий наглядное представление о максимально возможной сравнительной стойкости того или иного ВВ. Впервые такой анализ кинетики мономолекулярного распада ВВ был проведен Рогинским на основании собственных экспериментальных данных и материалов предшествовавших работ. [30]
Страницы: 1 2 3 4 5