Наблюдаемая зависимость - скорость
Cтраница 1
Наблюдаемая зависимость скорости рассматриваемой SE2 - реакции от природы заместителя X вполне понятна: влияние электроотрицательных заместителей выражается в появлении на атоме углерода, связанном со ртутью, частичного положительного, а влияние электроположительных - частичного отрицательного зарядов ( по-видимому, главным образом в момент реакции), сравнительно с незамещенным бензилмеркурбро-мидом. [1]
Наблюдаемая зависимость скорости расщепления от природы катиона металла, возможно, отражает разницу в константах диссоциации трех ттг етп-бутилатов в диметилсульфоксиде ( см. гл. [2]
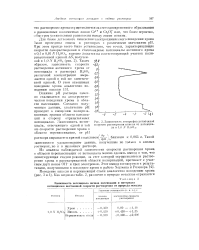 |
Зависимость логарифма устойчивой скорости растворения никеля от потенциала в 1 0 Л 1J2S04. [3] |
Из анализа наблюдаемой зависимости скорости растворения хрома в области перепассивации от потенциала можно сделать вывод о том, что лимитирующая стадия реакции, за счет которой осуществляется растворение хрома в рассматриваемой области поляризаций, протекает с участием двух ионов ОН - и трех электронов. [4]
Главной причиной разрушения скрытого изображения является окружающая среда, что очевидно из наблюдаемой зависимости скорости и степени регрессии изображения от условий хранения экспонированной непроявленной эмульсии. [5]
Известен большой класс ферментативных реакций, для которых уравнение Михаэлиса - Ментен не описывает экспериментально наблюдаемой зависимости скорости от концентрации субстрата. Эти случаи связаны со значительными изменениями в механизме реакции и, как правило, вызывают интерес исследователей, поскольку эффекты такого рода имеют большое регуляторное значение. Известно несколько механизмов, приводящих к неми-хаэлисовым зависимостям скорости реакции. Все эти механизмы связаны со взаимодействием с ферментом нескольких молекул субстрата. Отклонения могут быть вызваны ингибированием или активацией реакции избытком субстрата, а также аллостериче-скими эффектами. [7]
Уравнение Семенова широко используется при интерпретации экспериментальных данных по скоростям распространения медленных пламен [9, 10], однако оно неудовлетворительно предсказывает наблюдаемую зависимость скорости пламени от давления. Это уравнение также неприменимо для быстрых пламен, где определяющую роль играют цепные разветвленные реакции с участием атомов водорода. Высокая скорость таких пламен определяется не температурой горения или потоком тепла в исходную смесь газов, как в тепловой теории, и не скоростью диффузии исходных компонентов в зону реакции, как в диффузионной теории, а, скорее, скоростью, с которой активные центры - радикалы и атомы - диффундируют в горючую смесь и инициируют реакцию, ( в) Эта точка зрения была развита Тенфордом и Пизом [11, 12] в результате исследования скорости горения в смеси окиси углерода с кислородом. Оказалось, что скорость зависит от концентрации атомов водорода, которые приводят к цепному механизму реакции горения. [8]
Поскольку скорость реакции между Pu ( IV) и Fe ( II) обратно пропорциональна концентрации ионов водорода [15], может показаться, что это является причиной наблюдаемой зависимости скорости восстановления Pu ( IV) гидразином в присутствии Fe ( JIII) от кислотности. [9]
Поскольку при лимитировании процесса десорбцией цинка & дес2п мала, то мало и / ci, а следовательно, зависимость скорости процесса от Рсо будет невелика, и в предельном случае при очень малом ki мы найдем, что скорость восстановления не зависит от давления окиси углерода. Как видно, экспериментально наблюдаемая зависимость скорости процесса от давления окиси углерода находится в соответствии с зависимостью, описываемой уравнением ( 5), что подтверждает наше предположение о лимитирующей роли десорбции цинка. Смещение предела интенсифицирующего действия давления окиси углерода с повышением температуры в область более высоких давлений связано с соответствующим увеличением А дес. Повышение значения & Beczn приводит к росту ki, а тем самым к увеличению влияния давления окиси углерода на скорость восстановления. [10]
В этой модели приняты во внимание процессы на поверхностях горючего и окислителя, учтено различие средних высот и средних температур пламени над горючим и окислителем, различие в толщине слоев окислителя и горючего, а также отличие состава твердого топлива от стехиометри-ческого. Чтобы в этой модели получить наблюдаемую зависимость скорости горения от давления, необходимо ввести в рассмотрение либо экзотермическое гомогенное газовое пламя либо пламя разложения, примыкающее к поверхности одного из конденсированных реагентов, либо учесть процесс горения смеси горючего и окислителя в потоке после смешения. [11]
На практике известны оба случая. Поэтому для того чтобы объяснить наблюдаемую зависимость скорости окисления от структуры и стереохимии исходного соединения, необходимо рассматривать их влияние на обе стадии - образование промежуточного соединения и его распад. [12]
Для первых двух мономеров результаты согласуются с предположением о наличии реакции передачи цепи через растворитель, но в случае метилметакрилата требуемое значение ( kz) Mtta. Ясно, что в этом случае нужно искать другое объяснение наблюдаемой зависимости скорости полимеризации от концентрации мономера. В общем, предположение о передаче цепи через растворитель в данном случае допустимо только тогда, когда малые количества растворителя сильно замедляют полимеризацию. [13]
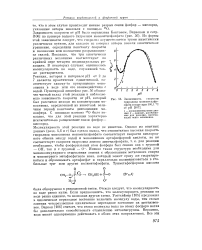 |
Зависимость скорости гидролиза мопометилфосфата в воде при 100 1 С от рН. 1 -экспериментальные данные. 2 -данные, рассчитанные для реакции, протекающей через моноанион. [14] |
Реакция, которая в интервале рН от 2 до 7 является практически единственной, соответствует какому-то превращению моноаниона в воде или его взаимодействию с водой. Пунктирной линией на рис. 56 обозначен чистый вклад этой реакции в наблюдаемую зависимость скорости от рН, который был рассчитан исходя из концентрации моноаниона, определенной из известной величины первой константы диссоциации моноэфира. С помощью изотопа 180 было показано, что для этой реакции характерно исключительно расщепление связи фосфор - кислород. [15]
Страницы: 1 2
