Ослабление - окраска
Cтраница 1
Ослабление окраски зависит от величины рН раствора. Оптимальное значение последнего-2 9; его фиксируют, прибавляя соответствующий буферный раствор, содержащий хлоруксусную кислоту и ее соль. [1]
Ослабление окраски зависит от величины рН раствора. Оптимальное значение последнего - 2 9; его фиксируют, прибавляя соответствующий буферный раствор, содержащий хлоруксусную кислоту и ее соль. [2]
Ослабление окраски раствора реактива в органической фазе пропорционально концентрации кальция в водной фазе. [3]
Это ослабление окраски связано с образованием бесцветного фенантролинового комплекса титана, о чем свидетельствуют спектры поглощения комплекса титана с ПАР в присутствии различных количеств фенантролина. Из рис. 19 видно, что по мере повышения количества фенантролина наблюдаются ослабление полосы поглощения окрашенного комплекса и усиление полосы поглощения свободного ПАР. [4]
Поразительно ослабление окраски антоцианидинов при переходе их в катехины. [5]
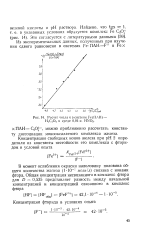 |
Расчет числа п в системе Ре ( ПАН - Н2С2О4 в среде 0 01 - н. HNO3. [6] |
В момент ослабления окраски наполовину половина общего количества железа ( Ы0 - 5 моль / л) связана с ионами фтора. [7]
Поэтому использование для ослабления окраски концентрированных серной и фосфорных кислот имеет смысл только при определении кремния в виде желтой SiMo, а не SiMo-сини, особенно при таком значительном избытке фосфора по сравнению с кремнием. [8]
При этом происходит ослабление окраски раствора реагента, что используется в фотометрическом анализе. Флотирующийся осадок, представляющий собой комплекс кальция с азо-азокси - БН, растворяется в некоторых полярных растворителях или в их смеси с неполярными. При этом кальций количественно извлекается в органическую фазу. [9]
Метод основан на ослаблении окраски комплекса, образующегося при рН 6 0 в присутствии пиридин солянокислого буферного раствора. [10]
Определение основано на ослаблении окраски соединения, образующегося при взаимодействии иона фтора с эриохромцианином и хлоридом циркония. [11]
Метод основан на ослаблении окраски цирконий-ализаринового комплекса при взаимодействии последнего с фтор-ионом. В зависимости от концентраций фтор-иона цвет раствора изменяется от слабо-розового до желтого. Данный метод применим для определения фторида в пределах 10 - 150 мкг в 100 мл анализируемого раствора. [12]
Метод основан на ослаблении окраски цирконий-ализаринового комплекса при взаимодействии последнего с фтор-ионом. [13]
При этом часто происходит ослабление окраски за счет обесцвечивания роданидного комплекса титана. [14]
Следует отметить, что ослабление окраски в результате разрушения комплексного соединения титана с перекисью водорода, а также комплексного соединения железа с роданид-ионом под действием фторид-ионов используют для количественного определения фторид-ионов. [15]
Страницы: 1 2 3