Металлический осмий
Cтраница 3
Оксифторид восьмивалентного осмия О5ОзР2, твердое желтое вещество ( температура плавления 170 С), гидролизующееся в четырехокись и фтористоводородную кислоту, синтезирован из четырехокиси осмия и трехфтористого брома или действием смеси фтора и кислорода на металлический осмий. [31]
При этом уже начинается восстановление до металлического осмия. Наконец, нагревают трубочку до красного каления, чтобы лишить осмий его пирофори-ческих свойств, вытесняют водород током углекислого газа и дают в нем остыть. [32]
Порошок металлического осмия, нагретый до 212 - 500 на воздухе, быстро превращается в летучую четырехокись осмия. На стенках сосудов, в которых хранится металлический осмий, оседает черный порошок Os02, который образуется в результате восстановления Os04 под действием следов органических соединений. [33]
Совместно с С. Е. Красиковым И. И. Черняев разработал метод получения металлического осмия из осмиевой кислоты, метод получения осмия высокой чистоты, метод получения чистого рутения, метод получения чистой платины, а также метод развески осмиевой кислоты. Некоторые из этих методов являются оригинальными научными работами и прочно вошли в практику аффинажа. [34]
Белая или желтая кристаллическая масса с сильным тошнотворным запахом. Весьма летуча, испаряется и при комнатной температуре, при которой медленно образуется, если металлический осмий распылен в воздухе. [35]
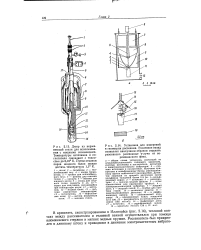
Источник прикреплен к вольфрамовому блоку, расположенному против конического рассеивателя. Детектор защищен от прямого излучения слоем вольфрама толщиной более 2 5 см. / - вольфрамовый экран; 2 - источник; 3 - рассеива-тель; 4 - полоска медной фольги; 5 - шток ( бакелитовая или пирексовая трубка); 6 - электромеханический вибратор; 7 - жидкий азот; 8 - жидкий гелий; 9 - трубки для протока гелия; 10 - свинцовая защита; / / - сцинтилляционный детектор; 12 - к диффузионному насосу; 13 - алюминиевый стержень; 14 - алюминиевый конус толщиной 0 15 мм, 15 - рассеиватель из металлического осмия ( 185 мг. [37]
В табл. 1 приведены результаты определения осмия при его содержании 5 мг. Однако при определении больших количеств осмия точность вполне приемлемая. Вес пробы в холостом опыте не пропорционален весу металлического осмия и зависит в значительной степени от количества реагентов и используемого объема раствора. [38]
Вербеной и соответствующий спирт - вербенол образуются также при автоокислении а-шшепа. Вербепол и вербеной являются продуктами разложения этой перекиси. Они образуются в больших количествах, если автоокисление происходит в присутствии металлического осмия. [39]
А как обстоит дело с газообразными окислами осмия. Здесь неравномерность распределения энергий конденсации не играет роли. И, как показали исследования последних лет, в парах над металлическим осмием в атмосфере кислорода присутствуют, в основном, OsO4 и ОзОз. И в газообразном состоянии уже двуокись осмия не выдерживает конкуренции с трехокисью, своим более экзотермическим в данном случае соседом. [40]
Частицы полимеров, содержащих ненасыщенные углерод-углеродные связи, например полидиены, протравливают путем обработки срезанных слоев парами тетраоксида осмия ( ОзС) или 2 % - ной осмиевой кислотой в течение 1 - 2 сут; это также способствует повышению контраста. При использовании такого метода становятся различимыми тонкие детали внутренней структуры ненасыщенных полимеров. Тетраоксид осмия реагирует с ненасыщенными двойными связями, окисляя их, при этом выделяется восстановленный металлический осмий и контрастность изображения улучшается. [41]
Частицы полимеров, содержащих ненасыщенные углерод-углеродные связи, например полидиены, протравливают путем обработки срезанных слоев парами тетраоксида осмия ( OsO4) или 2 % - ной осмиевой кислотой в течение 1 - 2 сут; это также способствует повышению контраста. При использовании такого метода становятся различимыми тонкие детали внутренней структуры ненасыщенных полимеров. Тетраоксид осмия реагирует с ненасыщенными двойными связями, окисляя их, при этом выделяется восстановленный металлический осмий и контрастность изображения улучшается. [42]
Около 60 лет тому назад Филлипс [54] установил, что четырехокись осмия легко восстанавливается этиленом, пропиленом, изобутиленом, ацетиленом и окисью углерода. Несколько позже Маковка [40] сообщил, что ацетилен более легко восстанавливает четырехокись осмия до черной низшей окиси, чем до металлического осмия. Вскоре после этого К. А. Гоф-манн [34] открыл, что водные растворы нейтральных хлоратов, являющиеся слабыми окислителями, могут гидроксилировать непредельные углеводороды в присутствии следов четырехокиси осмия. Впоследствии данная реакция была изменена и улучшена несколькими исследователями [8], которые определенно установили, что данная реакция, как и окисление перманганатом калия, является стереоспецифичной и ведет к образованию в больших количествах исключительно цис-а-гликолей. [43]
В лабораториях Os получают нагреванием диоксида осмия в атмосфере смеси водорода с двуокисью углерода; в технике его получают, извлекая из остатков платиновых руд после растворения их в царской водке. Этот остаток, содержащий осмий, рутений и иридий, сплавляют с цинком, прокаливают с пероксидом бария и экстрагируют водой избыток бариевых солей. Осадок подвергают перегонке с водяным паром. Осмий собирается в приемнике в виде осмиевой кислоты H2OsO4, из которой получают металлический осмий прокаливанием ее в графитовом тигле. [44]
Осмий легко сплавляется с другими платиновыми металлами, а также с железом, кобальтом и никелем. Также он образует хрупкие соединения с другими мегаллами: оловом и цинком. Порошкообразный осмий всегда обладает характерным запахом тетраоксида, потому что даже при комнатной температуре он окисляется на воздухе до OsO4, хотя и в слабой степени. Он - сильный окислитель и легко восстанавливается до диоксида ( OsOi) или даже до металлического осмия. Осмий также образует фториды OsF4, OsFe, и OsFg. Разнообразные хлориды образуются при обработке осмия хлором при высокой температуре. Реагируя с угарным газом, он образует карбонильные соединения. [45]
Страницы: 1 2 3 4