Близость - строение
Cтраница 3
На основании этого можно предположить, что Gd и Рг при высоких температурах образуют непрерывные ряды р твердых растворов, а при более низких температурах - непрерывные ряды а твердых растворов. При температурах ниже - 750 С образуется промежуточная фаза со структурой типа Sm, как и в других системах между легкими и тяжелыми лантанидами. Вследствие близости строения и атомных радиусов растворы Рг и Gd близки к идеальным, поэтому на диаграмме состояния системы Gd-Рг ( рис. 377) линии ликвидуса и солидуса, так же как и линии сольвуса, почти сливаются в прямые, соединяющие температуры плавления и превращения Рг и Gd с узкими двухфазными областями между ними. [31]
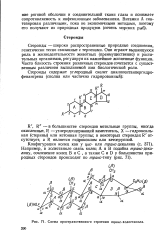 |
Схема пространственного строения тра г-холестанола. [32] |
Стероиды - широко распространенные природные соединения, генетически тесно связанные с терпенами. Они играют выдающуюся роль в жизнедеятельности животных ( преимущественно) и растительных организмов, регулируя их важнейшие жизненные функции. Часто близость строения различных стероидов сочетается с существенным различием выполняемой ими биологической роли. [33]
Молекулярный вес серу -, азот - и кислородсодержащих соединений обычно бывает близок к молекулярному весу углеводородов, которым они сопутствуют. По разнообразию в строении они не уступают углеводородной смеси. Их многочисленностью и близостью строения углеводородных радикалов к строению основного углеводородного состава нефтепродуктов объясняются трудности, возникающие при отделении неуглеводородных примесей ( особенно сер - нистых и азотистых соединений) от основной углеводородной) части топлив или масел. В настоящее время уделяют большое внимание разработке рациональных методов разделения. [34]
Кадмий оказывает выраженное действие на обмен ряда МЭ, в первую очередь цннка, медн, железа н селена. Это влияние проявляется на уровне ферментативных процессов, всасывания, отложения н выделения элементов, а также функции целого организма. Кадмиевое отравление в значительной степени зависит от его взаимоотношения с цинком. В связи с близостью строения атомов обоих элементов н сходством образуемых ими тетраэдрнческнх комплексов кадмий способен замещать цинк в хелатах этого металла н превосходит в этом отношении все остальные металлы, в том числе близкие к нему по химическим свойствам ртуть, медь н галлий. Исходя из этого кадмий можно рассматривать как специфический антимета-болнт цинка. Целый ряд токсических явлений, вызываемых действием кадмия, такие как гипертония, поражение кожных покровов, семенников, яичников, нервных ганглиев, удается в эксперименте предупредить одновременной дачей цинка. Хорошо известен антагонизм кадмия н по отношению к ряду других элементов. Удалось показать, например, что при избытке кадмия происходит обеднение организма животных медью и они погибают с выраженными признаками недостаточности меди [ Mills С. [35]
Для того чтобы избежать асимметричности и размытости пиков хроматограмм, необходимо было модифицировать поверхность твердого носителя. Для этого был испробован следующий способ модификации поверхности. На поверхность частичек диатомитового огнеупорного кирпича был нанесен диметилсилоксановый каучук с мол. Можно было ожидать, что большие молекулы каучука закроют доступ в наиболее мелкие поры твердого носителя, и поверхность его частиц, покрытая пленкой каучука, ненабухающего из-за большой степени вулканизации в неподвижной жидкости, будет хорошо смачиваться силиконовым маслом, вследствие близости строения молекул масла и каучука. [36]
Зависимость вязкости облученных водно-полимерных ( ПВС) растворов молибдата аммония имела вид, аналогичный системам жесткоцепный полимер - растворитель с образованием жидких кристаллов, с резким максимумом при повышении концентрации поливинилового спирта, отвечающим переходу от гомогенного состояния к гетерогенному, и последующим минимумом, характерным для жидкокристаллической фазы. В поляризованном свете под действием магнитного поля напряженностью были заметны полосчатые образования с периодом 10 - 20 мкм, которые служат признаком магнитного упорядочения в системе. Это позволило предположить, что в присутствии полимеров происходит взаимная стабилизация линейной формы макромоле-кулярных и солевых цепей, т.е. обнаружено новое явление: наведенная жесткость за счет комплексообразования неорганических полиионов с гибкоцепными водорастворимыми полимерами. Проявление замороженных мезофаз в твердом состоянии наблюдали на рентгеновских дифрактограммах измельченных пленок: на них присутствовал один узкий и интенсивный рефлекс, типичный для текстуры, образованной жидкокристаллическими объектами смектического типа. Установлен важный факт: период упорядочения для разных сочетаний соль - полимер был достаточно универсальным ( 0.316 - 0.320 нм), что может объясняться близостью строения координационных кислородных полиэдров для всех трех металлов. Признаки мезоморфизма проявляют другие системы, содержащие ПВС: с ванадатом и вольфраматом аммония. В настоящее время проводится работа по обобщению данных изучения разных систем для установления закономерностей взаимного влияния на растворимость полимера и соли, роли облучения в образовании мезоморфных структур. Получены данные о том, что полимерно-солевые пленки обладают сегнетоэлектриче-скими свойствами, что дало толчок новому циклу исследований. [37]
Растение это носит название Anabasis aphylla. О еем было известно только, что оно ядовито и что скот его не ест. Была установлена структура алкалоида, представляющая известную аналогию с никотином, с той лишь разницей, что в анабазине два шестичленных кольца, в отличие от пятичленного в никотине, и вторичный азот. Это строение было установлено на основе того, что при окислении анабазин дает никотиновую кислоту, а при дегидрировании - синтетически полученный а, 3-дипиридил. Этим была установлена структура анабазина, и мы перешли к изучению различных его производных. Близость строения анабазина к никотину, который давно применяется в качестве инсектицида, привела к мысли, что и анабазин может быть использован для этой цели. [38]
Двухвалентный никель захватывается в меньшей степени, чем трехвалентное железо. Отсутствие более или менее значительной адсорбции в ходе кристаллизации обусловлено большими скоростями роста кристаллов азотнокислого цезия, равными в рассматриваемом случае - 25 мк / мин. Как видно из табл. 23, степень захвата ионов лития оказалась почти в 8 раз больше, чем для меди и кобальта. Таким образом, остаются варианты, связанные с образованием твердых растворов. Образование такого раствора лимитируется близостью строения кристаллических решеток. С этой точки зрения наиболее близкими должны быть решетки нитратов лития и цезия. Но именно для лития наблюдается предельная концентрация, выше которой дальнейшая сокристаллизация прекращается. Между тем для азотнокислого кобальта свободно достигаются концентрации порядка 0.06 и приближения насыщения не чувствуется. Следовательно, образование коллоидных твердых растворов тоже вызывает сомнения. Остаются истинные твердые растворы, с образованием которых скорее всего и связана сокристаллизация примесей в данных условиях. Заметим, кстати, что ионные радиусы катионов примесей близки между собой. Их величины отвечают интервалу 0.57 - 0.82 А. Ионный радиус для цезия равен 1.65 А. Следовательно, отношения ионных радиусов колеблются в пределах 0.34 - 0.50. Но при образовании истинных твердых растворов играют роль не только ионные радиусы, но и валентность. С этой точки зрения в наиболее выгодном положении находится ион лития. Его внедрение в кристаллическую решетку азотнокислого цезия не ведет к образованию анионных или катионных вакансий. Захват ионов двухвалентных металлов связан с образованием одной катионной ва кансии, а трехвалентных - с двумя. Который из типов твердых растворов образуется - внедрения или замещения, - на основании одних лишь данных по сокри сталлизации сказать трудно. В главе VI показано, что образование твердых растворов внедрения более вероятно. [39]
Страницы: 1 2 3