Очень слабое основание
Cтраница 2
Соли очень слабых оснований частично гидролизуются, вследствие чего в использованном растворителе может находиться некоторое количество более слабого основания. [16]
 |
Аминоалканольные зфиры трициклических карбоновых кислот 15в. [17] |
Являясь очень слабым основанием ( растворы его имеют нейтральную реакцию), наркотин содержится в опии, главным образом, в свободном состоянии. [18]
Гидроксид висмута очень слабое основание, поэтому соли, висмута легко гидролизуются водой с образованием нерастворимых в воде основных солей. [19]
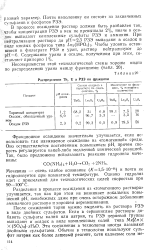 |
Распределение Th, U и РЗЭ по фракциям. [20] |
Мочевина - очень слабое основание ( / С 1 5 1 0 - 14) и почти не гидролизуется при комнатной температуре. Однако гидролиз идет с приемлемой для технологических целей скоростью при 90 - 100 С. [21]
 |
Электрофильное замещение в индоле3. [22] |
Индол - очень слабое основание ( рКа - 3, устойчивый катион образуется при протонированибЗ), и наиболее а не атома азота. Атом азота легко протонируени положения 3, тральном водном растворе, поэтому происходит тся даже в ней-водород - дейтерий, но реакция эта обратима и i быстрый обмен нуто в сторону непротонированной формы. [23]
Пиррол - очень слабое основание, поскольку свободная пара электронов, способная к образованию связи с протоном, делокализована. [24]
Для таких очень слабых оснований рН является важным параметром. Намного более сильные основания ( рК б) в аналогичных условиях практически полностью протонированы. На химически связанных фазах на основе силикагеля ионизацию этих соединений подавить невозможно и их следует разделять как ионы, используя либо ион-парную, либо ионообменную хроматографию. [25]
Для таких очень слабых оснований рН является важным параметром. На химически связанных фазах на основе силикагеля ионизацию этих соединений подавить невозможно и их следует разделять как ионы, используя либо ион-парную, либо ионообменную хроматографию ( см. разд. [26]
Для титрования очень слабых оснований в качестве растворителя часто выбирают ледяную уксусную кислоту, так как она обладает способностью быть донором протонов и увеличивает силу растворенных оснований. Выгодно также, что константа автопрото-лиза уксусной кислоты ( 3 6 - 10 - 15) несколько ниже, чем у воды. С другой стороны, в противовес этим преимуществам уксусная кислота обладает низкой диэлектрической проницаемостью. Два благоприятных свойства, однако, перевешивают единственный недостаток, и уксусная кислота является обычно лучшим растворителем для титрования слабых оснований. Ясно, что при титровании слабых кислот она будет уступать воде, поскольку обладает более слабыми протоноакцепторными свойствами. [27]
В случае очень слабых оснований соли их частично гидролизуются, вследствие чего в использованном растворителе может находиться некоторое количество более - слабого основания. [28]
 |
Схема дробного извлечения смеси двух оснований. [29] |
В случае очень слабых оснований соли их частично гидролизуются, вследствие чего в использованном растворителе может находиться некоторое количество более слабого основания. [30]
Страницы: 1 2 3 4