Очень слабое основание
Cтраница 3
Они являются очень слабыми основаниями и энергичными восстановителями, ас хл рангидридами кислот образуют замещенные гидцоксачовые кислоты, для которых характерна яркая окраска солей железа ( ср. [31]
Он является очень слабым основанием; органические растворители извлекают его даже из кислых растворов. Слабые основные свойства колхицина объясняются тем, что он является замещенным ацетамидом. Оказалось, что он содержит трополоновое кольцо ( стр. [32]
Ксантины являются очень слабыми основаниями и не образуют устойчивых солей с кислотами. Они дают кристаллические двойные соли с такими соединениями, как ацетат, бензоат или салицилат натрия; эти соли лучше растворимы, чем свободные основания. [33]
Пиррол является очень слабым основанием, так как неподеленная электронная пара атома азота участвует в образовании ароматического секстета и в координировании протона. Пиррол при растворении в концентрированных водных растворах минеральных кислот полимеризуется, поскольку при протонировании эта электронная пара удаляется из электронного секстета ядра и молекула приобретает диеновую структуру. [34]
Дифениламин является очень слабым основанием, соли которого гидролизуются водой. [35]
Имиды являются очень слабыми основаниями, в этом они сравнимы со спиртами и эфирами. [36]
Поскольку SbfOHb - очень слабое основание, соли Sb3 подвержены гидролизу. [37]
Амиды представляют собой очень слабые основания, слишком слабые, чтобы атаковать алкилгалогениды, поэтому вначале их необходимо превратить в сопряженные основания. [38]
Оксициннолины представляют собой очень слабые основания. [39]
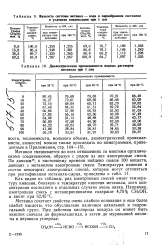 |
Вязкость системы метанол - вода в парообразном состоянии в условиях конденсации при 1 am.| Диэлектрическая проницаемость водных растворов метанола при 1 am. [40] |
Метанол сочетает свойства очень слабого основания и еще более слабой кислоты, что обусловлено наличием алкильной и гидрок-сильной групп. [41]
Для определения силы очень слабых оснований Гаммет использовал последовательный ряд кислых растворителей, таких, как смеси соляной, азотной, хлорной или серной кислот с водой. Предположим, что в качестве эталонного основания В выбран индикатор, для сопряженной кислоты которого ВН известна термодинамическая константа диссоциации в воде Ка-Для определения силы несколько более слабого основания С в качестве растворителя может быть использована 10 % - ная серная кислота. Основания В и С и растворитель подбирают таким образом, чтобы можно было измерить соотношения концентраций В / ВН и С / СН в выбранном растворителе. [42]
Амиды кислрт являются очень слабыми основаниями; это объясняется тем, что электронная пара азота смещена в сторону карбонильной группы, обладающей большим - С-эффектом. В результате основность азота у амидов уменьшена, а основность кислорода - увеличена. [43]
Амиды кислот являются очень слабыми основаниями; это объяс-шется тем, что электронная пара азота смещена в сторону карбониль-юй группы, обладающей большим - С-эффектом. Ацетамид в сухом фире дает очень непрочную соль с НС1, гидролизующуюся при рас - ворении в воде. [44]
Оз - являются очень слабым основанием ( р / с2 2), поэтому выделяющиеся ионы CN можно титровать кислотой. [45]
Страницы: 1 2 3 4