Пуриновое пиримидиновое основание
Cтраница 2
 |
Состав рибосомных РНК эукариот. [16] |
Здесь и далее пуриновые и пиримидиновые основания обозначены начальными буквами соответствующего названия. [17]
Разная радиочувствительность пуриновых и пиримидиновых оснований объясняется различием их химической структуры. У пуриновых оснований наиболее легко насыщаемая связь 4 - 5-пиримидинового цикла защищена имидазольным кольцом. Ее насыщение происходит после размыкания этого кольца уже в составе продукта первичной реакции - пиримидинового форма-мидопроизводного, образование которого можно рассматривать как потерю оснований, так как с этой реакцией связано ускорение распада пуриновых хромофоров. [18]
Эквивалентное отношение пуриновых и пиримидиновых оснований в ДНК было объяснено Уотсоном и Криком ( 1953 г.), предположившими, что две цепи ДНК построены так, что при их сплетении в двойную спираль образуются водородные связи между адени-ном в одной цепи и тимином в другой или аналогично между цитозином и гуанином. [19]
Синтетические аналоги пуриновых и пиримидиновых оснований, нуклео-зидов, нуклеотидов находят широкое применение в молекулярной биологии, фармации и медицине. Их использование связано в первую очередь со структурной ролью нуклеотидов как предшественников синтеза нуклеиновых кислот. [20]
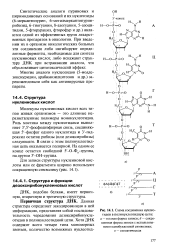 |
Схема соединения нуклео. [21] |
Синтетические аналоги пуриновых и пиримидиновых оснований и их нуклеозиды ( 6-меркаптопурин, 6-метилмеркаптопурин-рибозид, 6-тиогуанин, 8-азогуанин, 5-азоци-тидин, 5-фторурацил, фторофур и др.) являются одной из эффективных групп лекарственных препаратов в онкологии. При введении их в организм онкологических больных эти соединения либо ингибируют определенные ферменты, необходимые для синтеза нуклеиновых кислот, либо искажают структуру ДНК при встраивании аналога, что обусловливает цитотоксический эффект. [22]
Более половины пуриновых и пиримидиновых оснований тРНК с помощью водородных связей образуют внутрицепо-чечные пары по принципу комплементарности ( А-1 ] С-С, О-О; О и О-соотв. Эти короткие спирали чередуются с участками неспаренных оснований, в результате чего нуклеотидная цепь образует 3 петли. Таким образом формируется вторичная структура, получившая назв. В ней выделяют: акцепторную ветвь ( стебель, черешок) с универсальной З - концевой последовательностью, служащей акцептором ( местом прикрепления) остатка аминокислоты; дигидроуридиловую ветвь ( шпильку), варьирующую по числу входящих в ее состав нуклеотидов и содержащую до 3 остатков дигидро-уридина ( ВНЦ); антикодоновую ветвь ( шпильку) с петлей в 7 нуклеотидных остатков, в центре к-рой находится анти-кодон ( тринуклеотид, комплементарный ко дону мРНК и обусловливающий специфичность тРНК к этому кодону); тимидилпсевдоуридиловую ветвь, или Ту-шпильку, содержащую минорные нуклеозиды риботимидин и псевдоури-дин. [23]
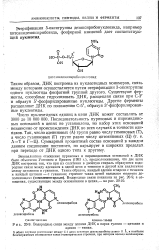 |
Водородные связи между цепями ДНК в парах гуанин - цитозин и. [24] |
Эквивалентное отношение пуриновых и пиримидиновых оснований в ДНК было объяснено Уотсоном и Криком ( 1953 г.), предположившими, что две цепи ДНК построены так, что при их сплетении в двойную спираль образуются водородные связи между аденином в одной цепи и тимином в другой или аналогично между цитозином и гуанином. [25]
Химическое строение пуриновых и пиримидиновых оснований, а также углеводов, входящих в состав нуклеиновых кислот, показано на следующей странице. [26]
Готовят раствор свободных пуриновых и пиримидиновых оснований ( 2 мг / мл) в 10 % - ном растворе изопропаиола, к которому добавляют 10 % уксусной кислоты. [27]
Здесь буквы изображают пуриновые и пиримидиновые основания. [28]
В биологическом материале свободные пуриновые и пиримидиновые основания встречаются в небольших количествах. Они, как известно, являются компонентами дезоксирибонуклеиновых и нуклеиновых кислот и освобождаются при их гидролитическом расщеплении. [29]
Путем исследования растворов пуриновых и пиримидиновых оснований и соответствующих нуклеозидов и нуклеотидов была изучена химическая природа радикальных реакций с нуклеиновой кислотой. Если облучение проводится в присутствии молекулярного кислорода, то в значительной степени происходит реакция образования пероксисоединений из пиримидиновых оснований и в особенности из тимина и урацила. [30]
Страницы: 1 2 3 4