Основность - среда
Cтраница 2
При недостаточном сдвиге равновесия вправо необходимое повышение основности среды для исключения побочного процесса достигается проработкой электролита током. Во время такой проработки в диффузионном слое раствора у поверхности катода содержание ионов НЭ значительно понижается за счет электролитического выделения водорода, в результате чего донорное воздействие основания быстро увеличивается. [16]
Кислотно-основные равновесия более чувствительны к изменению диэлектрической проницаемости и основности среды. При уменьшении диэлектрической проницаемости приобретает значение образование ионных пар или ассоциатов более высокого порядка. Кортюм и Андрусов [29] нашли, что относительно неустойчивые ионные пары Бьеррума, присутствующие в метанольных растворах, спектроскопически неразличимы от свободных ионов. В апротонном растворителе, например бензоле, свободные ионы, возможно, не играют значительной роли во взаимодействии кислот и оснований, несмотря на перемену окраски индикатора. [17]
Реакция протекает достаточно быстро при рН 8 2; с увеличением основности среды скорость восстановления уменьшается. Продукт реакции легко окисляется под действием нитрита натрия при рН 5 4; в щелочной среде происходит окисление под действием кислорода воздуха, которое сопровождается перегруппировкой Дим-рота ( см. стр. [18]
Из этих данных вытекает существование закономерной связи между интенсивностью хемилюминесценции и основностью среды, а именно с повышением рН среды интенсивность увеличивается, что согласуется с представлениями о раскрытии цикла пиридиния в основных средах. [19]
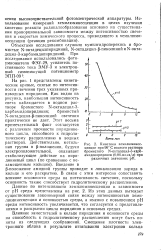 |
Кинетика хемилюминесценции при 90 С водного раствора бромистого N-октадецил - З - карб-амидопиридиния ( 0 04 моль / л при различных значениях рН. [20] |
Из этих данных вытекает существование закономерной связи между интенсивностью хемилюминесценции и основностью среды, а именно с повышением рН среды интенсивность увеличивается, что согласуется с представлениями о раскрытии цикла пиридиния в основных средах. [21]
В любом случае прибавление фтористого водорода должно уменьшать скорость рацемизации, понижая основность среды. Этот эффект должен быть ( и является) сильнее в пентане, чем в mpem - бутиловом спирте. [22]
Полученные результаты ( табл. 7.4) свидетельствуют о том, что увеличение основности среды и исключение гидроксилсодержащего растворителя приводит к возрастанию содержания пара-изомера. [23]
При большом избытке катализатора ускоряется гидролиз хлорформиатных групп, в результате чего повышается основность среды, и, следовательно, группы - ОСООН будут образовываться быстрее, чем расходоваться в реакциях с катализатором и хлорфор-мпатными группами. [24]
При большом избытке катализатора ускоряется гидролиз хлорформиатных групп, в результате чего повышается основность среды, и, следовательно, группы - ОСООН будут образовываться быстрее, чем расходоваться в реакциях с катализатором и хлорформиатными группами. [25]
Изменить величину КИЭ можно, не только изменяя природу основания, но и изменяя основность среды, например, путем добавления ДМСО к протонным растворителям. На эту возможность впервые было указано Сондерсом [180] и Джонсом [177], а экспериментальные доказательства получены Коккериллом [181] для реакции элиминирования олефинов, Беллом [182] для инверсии ментона в щелочных средах и Бергманом [19] при исследовании рацемизации 2-фенилпропионитрила. [26]
При большом избытке катализатора он, по-видимому, ускоряет гидролиз хлорформиатных групп, повышая основность среды. В результате концентрация групп - ОСООН возрастает быстрее, чем они расходуются на реакцию с катализатором и последующую реакцию с хлорформиатными группами. При увеличении избытка щелочи в системе оптимальная концентрация катализатора при оптимальном избытке фосгена уменьшается. [27]
Более детальное исследование циклоароматизации показало, что направление реакции зависит от природы растворителя, основности среды и природы катиона металла в алкоголяте. [28]
В дальнейшем удалось установить, что перегруппировка идет по двум направлениям одновременно, а степень основности среды определяет лишь главное из них. На основании проведенных исследований общая картина превращений 3.4 - дигидро-4 - сульфокислот нафтофуроксана в щелочной среде представляется следующим образом. [29]
 |
Зависимость вязкости раствора полиарилата диана и терефталевой кислоты в смеси тетрахлорэтан - фенол от количества в межфазной поликонденсации катализатора тетра-этиламмонийхлорида. [30] |
Страницы: 1 2 3 4