Отклонение - реальный газ
Cтраница 2
Причины отклонений реальных газов от законов, выведенных для идеальных, голландский ученый Ван-дер - Ваальс ( 1873) объясняет следующим образом. Молекулы газа, заключающиеся в данном его объеме v, всей своей совокупностью создают некоторое несжимаемое пространство Ь, называемое коволюмом. Величина коволюма, согласно Ван-дер - Ваальсу, равна учетверенному сплошному объему самих молекул. [16]
Причина отклонения реальных газов от законов газового состояния заключается в следующем. [17]
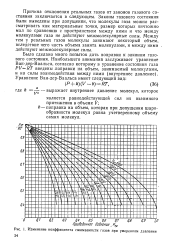 |
Изменение коэффициента сжимаемости газов при умеренном давлении 24. [18] |
Причина отклонения реальных газов от законов газового состояния заключается в следующем. Законы газового состояния были выведены при допущении, что молекулы газа можно рассматривать как материальные точки, размер которых ничтожно мал по сравнению с пространством между ними и что между молекулами газа не действуют межмолекулярные силы. Между тем у реальных газов молекулы занимают некоторый объем, вследствие чего часть объема занята молекулами, и между ними действуют межмолекулярные силы. [19]
Коэффициент отклонения реальных газов от законов идеальных принят средним для всех участков. Формула (1.25) позволяет рассчитать горизонтальный газопровод с отбором газа по длине. [20]
Рассмотрим влияние отклонений реальных газов от законов идеальных газов и изменения вязкости на истощение газовых залежей. [21]
Рассмотрим влияние отклонений реальных газов от законов идеальных газов и переменности вязкости на истощение газовых залежей. [22]
Фактор сжимаемости учитывает отклонения реального газа от уравнения состояния идеального газа ( уравнение Менделеева - Клапейрона) и представляет собой функцию температуры и давления, или функцию приведенных температуры и давления, а для смесей - функцию псевдоприведенной температуры и давления. [23]
При давлении 250 атм отклонение реального газа от идеального представляет собой значительную величину, в связи с чем в уравнение равновесия процесса необходимо вводить поправку на фугетивность. [24]
Остановимся кратко на причинах отклонения реальных газов от законов идеальных газов. [25]
В области высоких давлений отклонения реальных газов от уравнений ( 1), ( 2) настолько значительны, что пренебречь ими нельзя. [26]
К - коэффициент, учитывающий отклонения реального газа от идеального газа ( коэффициент сжимаемости газа); при давлении, меньшем 0 49 Мн / м2 ( 5 кГ / см2), и температуре ниже 50 С коэффициент К практически равен единице для всех газов. [27]
Кроме описанного упрощенного способа учета отклонения реальных газов от состояния идеального с помощью коэффициента сжимаемости существуют другие методы, позволяющие учитывать отклонения законов реального от законов идеального газа. [28]
Ошибки этих методов, обусловленные отклонением реальных газов от законов идеального газа, могут быть уменьшены применением более точных ур-ний состояния вместо ур-ния Клапейрона. Все эти методы применимы и к смеси газов. [29]
Дер является корректирующим членом, учитывающим отклонения реального газа от идеального. [30]
Страницы: 1 2 3 4