Падение - энергия - активация
Cтраница 1
Падение энергии активации в области 25 - 35 С показывало, что при такой полимеризации существовала некоторая стадия предравновесия. Похоже на то, что в данном случае имел место тот же самый индукционный период, который наблюдался другими исследователями при подобных условиях при 25 С, являющийся первой стадией формирования некоторых полимерных разновидностей малого размера, с которыми затем более предпочтительно вступает во взаимодействие мономерный кремнезем. [1]
Падение энергии активации с температурой мы объясняем повышением с температурой активности углеродной поверхности. При достаточно высокой температуре энергия поверхностных атомов оказывается настолько значительной, что они способны вступить в реакции с молекулами газа, энергия которых меньше, чем теплота протекающей эндотермической реакции. И даже сильно эндотермические реакции ( например, С СО2) при достаточно высокой температуре способны протекать при энергии активации, близкой к нулю. [2]
При повышении давления скорость реакции возрастает в результате падения энергии активации. [3]
Подобные отклонения в ряде случаев могут быть следствием и других причин, вызывающих падение энергии активации с ростом температуры. К ним относится, например, частичное вырождение ионных связей в гомеополярные, наблюдаемое при высоких температурах у галогенидов, а также разрушение крупных комплексных анионов на более простые. [4]
 |
Энергии активации реакций соединения О с Н2О и NO с О2 и СЬ. [5] |
Интересно, что увеличению экзоэффекта при переходе от реакции NO с хлором к реакции с кислородом отвечает падение энергии активации. [6]
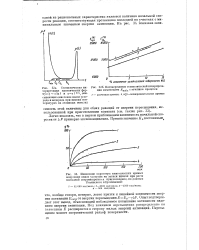 |
Подтверждение статистической интерпретации изменением. Енадл с течением процесса.| Изменение характера кинетических кривых. [7] |
Енабл от энергии пересыщения Е - Е0 - уд - Опыт подтверждает этот вывод, объясняющий наблюдаемое повышение активности падением энергии активации. Под влиянием пересыщения распределение по значениям Е расширяется в сторону малых энергий активаций. Пересыщение меняет энергетический рельеф поверхности. [8]
Очевидно, что иррегулярное изменение скоростей реакции обусловлено сочетанием более регулярных изменении энергии акти-нацни и вероятностного фактора. Падение энергии активации от трех - к пятичленным кольцам является мерой падения напряжения, возникающего яри сближении концов цпклизующейся системы. Ifc совсем ясно, почему возрастает напряжение при образовании шестичленного кольца. Вероятностный фактор очень высок для трехчленного кольца, так как любое расположение атомов и трехчленной цени одинаково благоприятно для циклизации. Несколько более высокий вероятностный фактор для нятичлонного кольца рассматривается как признак бол ыпей склонности пятичленнон цепи существовать в кольцеобразной ( а не зигзагообразной) конфор-мации по сравнению с цепью из четырех или шести атомов. В этой конформации концы цепи легко сближаются друг с другом. Циклы от восьмичленного до четырнадцатичлепного нельзя получить никакими способами, кроме ацилоинового синтеза, поскольку атомы в этих циклах располагаются таким образом, что возникает либо трансаинуляриое пространственное взаимодействие водородных атомов ( СН2 - групн), либо коиформацнонное напряженно за счет противостояния связей соседних метиленовых групп ( см. гл. Циклы от четырнадцатичлеиного и выше образуются легче, хотя, конечно, вероятность, что концы такой системы сблизятся, незначительна. [9]
 |
Области стеклообразования в тройных системах, содержащих CuSO4, T12SO4, K2SO4 и ZnSO4. [10] |
Предполагают, что разрушение конфигурационной упорядоченности, обычно происходящее при плавлении, здесь не завершается при температуре, близкой к температуре плавления. Считают, что падение энергии активации при 210 указывает на завершение этого процесса. [11]
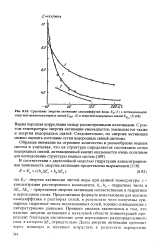 |
Сравнение энергии активации самодиффузии воды ED ( 1 с потенциальной энергией межмолекулярных связей EMD ( 2 и энергией водородных связей Ен ( 3. [12] |
Предложенная формула использована для анализа самодиффузии в растворах солей, в результате чего получены суммарные гидратные числа исследованных солей, хорошо совпадающие с литературными данными. Принцип анализа заключался в том, что падение энергии активации в начальной области концентраций происходит благодаря увеличению доли переходного разупорядоченного слоя, в котором А. [13]
В связи с тем, что для этих реакций наблюдается падение энергии активации с температурой, применение метода Аррениуса приводит к получению неверных результатов, чем и объясняется широкий диапазон значений энергии активации, полученных многими авторами. К сожалению, несмотря на большое число работ по горению и газификации углерода, очень немногие работы содержат данные об абсолютной скорости реакции, отнесенной к единице реагирующей поверхности. Результаты, полученные в этих работах, были применены нами для молекулярно-кинетнческого расчета энергии активации, как это было сделано выше для реакций образования углерода при термическом разложении углеводородов. [14]
Формула ( 3) определяет максимальную крутизну кривой Е ( Т), при которой отклонение от закона Аррениуса будет меньше погрешности измерений. Покажем, что формально такой крутизны достаточно для того, чтобы обеспечить в разумном интервале температур AT ( - 200 С) падение энергии активации на 26 ккал / моль и увеличение эффективной энергии активации до 65 ккал / моль. [15]
Страницы: 1 2