Бойда
Cтраница 1
Бойда посвящена быстро развивающемуся разделу науки, лежащему на стыке иммунологии, химии, микробиологии и биохимии. [1]
Бойда не лишена недостатков; так, например, слишком конспективно изложены данные о химии антител. Однако эти недостатки полностью искупаются тем, что автор сумел изложить современные данные по химии антител очень живо, в форме, доступной для широкого круга биологов, медиков и химиков. Очень удачное оформление книги - большое число наглядных схем и рисунков - облегчает понимание материала. [2]
Бойд и Ингланд [11, 12] изучили зависимость температуры плавления диопсида до давления 60 кбар. [3]
Бойд и Солдано [ 361 нашли, что сульфополистирольные смолы имеют очень низкое давление паров при комнатной температуре, если содержание воды в них мало. [4]
Бойд, А дам сон, М е и е р с, сб. [5]
Бойд Р Органическая химия Пер с англ / Под ред И К Коробнцнной М Мир. [6]
Бойд, Эвергарт и Мак-Мастер обнаружили, что некоторые препараты, получаемые из Bauhinia purpurea и являющиеся неспецифическими ( вернее, специфическими по отношению к сахарам, относящимся к 2 - й группе), могут быть превращены в N-специфические путем добавления D-галактозы или иных Сахаров 2 - й группы. Однако большинство неспецифических, растительных агглютининов при подобной обработке ингибирующи-ми сахарами не проявляет новой специфичности. Упоминавшиеся выше три лектина в этом отношении представляют, видимо, исключение. [7]
Бойд и Ливингстон30, применив уравнения Бингама и Резаука [ см. уравнения ( 8) и ( 14) ] так же, как это в последующем сделали Харкинс и некоторые другие исследователи14 7в 95, рассчитали величину WA для воды, пропанола, пропилацетата, ацетона, бензола и н-гептана на поверхностях кварца ( SiO2), анатаза ( ТЮ2), сульфата бария ( BaSO4), двуокиси олова ( SnO2), окиси железа ( Fe2O3), графита, ртути, меди, серебра, свинца, железа и олова. Для каждой из этих систем по изотермам адсорбции паров на соответствующей твердой поверхности была рассчитана величина / sv -; оказалось, что ею пренебрегать нельзя, так как в каждом случае по порядку величины она совпадала с WA - В каждом из перечисленных выше случаев твердые тела представляли собой тонко раздробленный материал и, за исключением графита, являлись гидрофильными адсорбентами с поверхностью высокой энергии. [8]
Бойд и Хаттон [39] исследовали пригодность кварцевых пластинок в качестве подложек для тонкого слоя кремневой кислоты, с тем чтобы рассматривать полученные хроматограммы в проходящем УФ-свете. Однако оказалось, что слой кремневой кислоты настолько сильно поглощает, что пятна на хромато-грамме мало отличаются от фона. [9]
Бойд полагает, что водород в сплаве Ti - 8А1 - IMo - IV находится в пересыщенном а-твердом растворе. Гидриды не выделяются из пересыщенного водородом раствора, поскольку алюминий резко затрудняет образование зародышей гидридов. Но, как только зародыши образовались ( в сплаве Ti - 8А1 - IMo - IV это происходит при концентрации водорода 0 08 %), начинается быстрый спонтанный распад пересыщенного водородом раствора. При 0 08 % Н2 содержание гидридов в сплаве составляло 2 5 %, а это означает, что истинная растворимость водорода в а-фазе очень мала - такая же, как в а-титане, или даже меньше. [10]
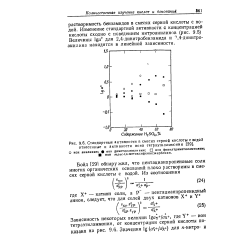 |
Стандартные активности в смесях серной кислоты с водой. [11] |
Бойд [ 291 обнаружил, что пентацианпропеновые соли многих органических оснований плохо растворимы в смесях серной кислоты с водой. [12]
Бойд и Бернштейн [28], используя в работе меченые атомы, показали, что щелочные соли не повышают, а понижают адсорбцию поверхностно-активных веществ как волокнами, так и загрязнениями, особенно это относится к конденсированным фосфатам. Авторы считают, что на основании адсорбции поверхностно-активных веществ волокнами в присутствии щелочных солей невозможно предложить теорию о механизме их действия. [13]
Бойд и Менис [171] показали, что уран ( IV) может окисляться до урана ( VI) при положительных потенциалах, больших чем 0 5 в, несмотря на тот факт, что переход уран ( IV) - уран ( VI) необратим; для аналитических целей они рекомендовали применять потенциал 1 4 в. [14]
Бойд, Адамсон и Майерс [52], помимо влияния зернения сорбента и скорости течения раствора, детально изучили и влияние концентрации ионов в растворе; они показали, что в 0 1 М и более концентрированных растворах скорость ионного обмена определяется внутренней диффузией, а в 0 001 М и более разбавленных - внешней диффузией. [15]
Страницы: 1 2 3 4