Педерсен
Cтраница 3
Исходя из данной гипотезы, Педерсен синтезировал 49 макроциклических полиэфиров с 9 - 60-членными кольцами, содержащих от 3 до 20 эфирных фрагментов. В их числе получено 33 макроцикла, содержащих ароматические кольца, 15 макроциклов с алиииклическими кольцами, синтезированных гидрированием ароматических колец, и циклический гексамер этиленоксида. [31]
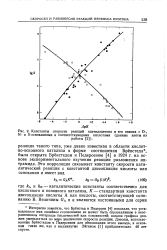 |
Константы скорости реакций ацетилацетона и его аниона с О -, N - и S-основаниями и соответствующими кислотами ( данные взяты из. [32] |
Интересно заметить, что Бренстед и Педерсен [4] показали, что установленное ими линейное соотношение не может быть справедливым в неограниченном интервале кислотностей или основностей; наклон графика должен уменьшаться по мере увеличения скорости реакции. Доводы, использованные Бренстедом и Педерсеном для обоснования этого вывода, в основном такие же, как и выдвинутые Зйгеном ДО ] приблизительно 40 лет спустя. [33]
Для целей такого рода сравнений Бренстед и Педерсен приняли константу кислотности ионов лиония равной Сц, а константу кислотности растворителя равной Kjcw wr i. [34]
Хьертен и Мосбах [8], а также Педерсен [22] высказали предположение, что аналогичное явление может наблюдаться при хроматографии на молекулярных ситах, однако экспериментального подтверждения этому еще не дано. [35]
В 1920 - х годах Бренстед и Педерсен получили экспериментальные данные, показывающие, что чем сильнее соединение А Н ( или Bj) как кислота ( или основ ание), тем оно эффективнее как общий кислотный ( основной) катализатор. Это означает, что поведение кислот и оснований при ионизации ( обмен протона с растворителем) тесно связано с их поведением как общих кислотных и основных катализаторов. Соотношение межу силой кислоты или основания и скоростью катализируемых ими реакций называется каталитическим законом Бренстеда. [36]
Начало химии макроциклических полиэфиров принято датировать 1967 г., когда Педерсен [29] осуществил синтез 33 соединений, различающихся размером макрокольца и количеством эфирных донор-ных атомов. [37]
Что неположительность кривизны является более сильным условием, чем выпуклость оболочек, заметил Педерсен [1]; в этой же работе имеется перенесение многих теорем на пространства с выпуклыми оболочками. [38]
Такая беспрецедентная эффективность замыкания восемнадцатичленного цикла в одну операцию в результате взаимодействия двух молекул 212 с двумя молекулами 213, причем без применения техники высокого разбавления ( обычно необходимой для успешной макроциклизации, см. разд. Педерсен справедливо счел этим фактором матричный эффект иона натрия, вокруг которого в качестве лигандов группируются все четыре молекулы. Позже Педерсен рассказывал: Мои первые действия мотивировалось скорее эстетикой, чем наукой. [39]
Такая беспрецедентная эффективность замыкания восемнадцатичленного цикла и одну операцию в результате взаимодействия двух молекул 212 с двумя молекулами 213, причем без применения техники высокого разбавления ( обычно необходимой для успешной макроциклизации, см, разд. Педерсен справедливо счел этим фактором матричный эффект иона натрия, вокруг которого в качестве лигандов группируются все четыре молекулы. Позже Педерсен рассказывал: Мои первые действия мотивировалось скорее эстетикой, чем наукой. [40]
Педерсен синтезировал 49 макроциклических полиэфиров с 9 - 60-членными кольцами, содержащих от 3 до 20 эфирных фрагментов. В их числе получено 33 макроцикла, содержащих ароматические кольца, 15 макроциклов с алиииклическими кольцами, синтезированных гидрированием ароматических колец, и циклический гексамер этиленоксида. [41]
Алициклические краун-эфиры, содержащие одно или более насыщенных алифатических колец, например Дициклогексил-18 - краун-6, обычно получаются гидрированием соответствующих ароматических краун-эфиров. Педерсен [ 4] этим способом получил 13 алициклических краун-эфиров. [42]
Педерсен открыл краун-эфиры и обнаружил эти свойства, которые обеспечили основу развития химии и применения краун-соединений. Педерсен [ 1] синтезировал ряд краун-эфиров и установил, что в органических растворителях в их присутствии можно растворять различные неорганические соли. Впоследствии он подтвердил рядом методов, включая изменения в УФ-спектрах, что между краун-эфирами и неорганическими солями образуются комплексы. Педерсен выделил также ряд кристаллических комплексов и установил их структуру путем анализа состава этих комплексов и сравнением относительных размеров полости краун-эфира и ионного диаметра катионов металла. [43]
 |
Типы структур комплексов различных краун-эфиров с ионами Na и К (. аоопроизведено с любезного. [44] |
Помимо катионов металлов, перечисленных в табл. 3.4, комплексы с краун-эфирами образуют также ионные и полярные органические соединения. Педерсен [1] обнаружил, что соли RNH, такие, как HONH3C1, NH2NH3C1, ( CH3) 2CHCH2NH3CL, ( CH3) 2CHCH2CH2NH3C1, ( CH3) 3CNH3CL PhNH3Cl, NH3CH2CH2NH3C1, HOOCCI NHgCl, [ NH2C ( NH2) NH2 ] C1, [ NB C ( NH2) NH2 ] 2 - - C03, образуют комплексы с дибензо-18 - краун-6 в метаноле. Крам и др. [27] сообщили о комплексообразовании между солями гуанидиния и дибензо-27 - краун-9, о чем говорилось ранее в разд. [45]
Страницы: 1 2 3 4