Пентафторид
Cтраница 4
В 1963 г. был впервые получен пентафторид хлор. Это - жидкость, затвердевающая при - 93 С, температура кипения 129; ее, наряду с такими веществами как NF2O2, ClzO8, NF OONF2, называют суперокислителвм. [46]
Пентахлорид фосфора может быть превращен в пентафторид нагреванием с пентафторидом сурьмы ( уравнение 35) и другими фторирующими реагентами. Замещение первого атома фтора протекает быстро, второй атом фтора замещается медленнее и на этой стадии реакция останавливается. [47]
 |
Прибор для получения пентафторидов. [48] |
При атмосферном давлении ниобий образует только пентафторид, а тантал, также и некоторое количество нелетучего трифторида. [49]
Добавки кислоты Льюиса служат для вытеснения пентафторидов металлов из их неактивных комплексов. Если применяемая кислота Льюиса сама не является фторидом, то происходит обмен галогена и образуются пентагалогениды тантала и ( или) ниобия. До проведения дистилляции из катализатора может быть также удален пентафторид металла, не связанный в комплекс. [50]
Кларк и Эмелеус [113] изучили реакции пентафторидов ванадия, ниобия и тантала с нитрил фторидом, нитрозилфторидом и че-тырехокисью азота в трифториде брома. [51]
Из соединений хлора ( V) известны пентафторид C1F6, диоксофтопид C102F и производные [ С1О3 ] - - тржжсохлорат ( V) - и [ C1O3F ] 2 - - триокссфторо-хлорат ( У) - комплексов. Пентафторид хлора еще менее устойчив, чем C1F3 и его свойства пока плохо изучены. Ведутся исследования по получению производных [ C1F6 ] - - комплекса. [52]
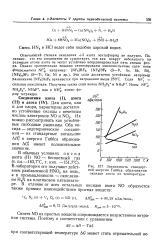 |
Зависимость стандартной энергии Гиббса образования оксидов азота от температуры. [53] |
Отвечающий степени окисления 4 - 5 азота пентафторид не получен. Полагают, что это соединение не существует, так как вокруг небольшого по размерам атома азота не могут устойчиво координироваться пять атомов фтора. Эти соли достаточно устойчивы: например разложение [ NF4 ] AsFc начинается при нагревании выше 250 С. NH, имеют форму тетраэдра. [54]
Будучи менее полярными, чем трифториды, пентафториды мышьяка, сурьмы и висмута плавятся и кипят при более низких температурах, чем трифториды. [55]
Из галогенидов ЭГ известны только пентагалогениды: пентафторид ванадия VF6, пентафторид, - хлорид, - бромид ниобия NbF5, NbCl6, NbBrj и пентафторид, - хлорид, - бромид, - иодид тантала TaFg, ТаСЦ, TaBrg, Talg. [56]
Так же можно объяснить отсутствие у азота пентафторида, тогда как для фосфора соединение PF5 вполне устойчиво. [57]
Окисление проводят при ультрафиолетовом облучении смеси хлорида пентафторида серы и кислорода ( 3: 1) при атмосферном давлении в течение 6 час. При этом образуется некоторое количество перекиси биспентафторида серы. [58]
Страницы: 1 2 3 4