Пентахлорид - ниобий
Cтраница 1
Пентахлорид ниобия из испарителя через вентиль тонкой регулировки 13 подается в камеру, в которой смешивается с рабочей газовой смесью и поступает в реакционную камеру. [1]
Пентахлорид ниобия отгоняется из зоны реакции, а в остатке получается чистая хлорокись алюминия. [2]
Пентахлорид ниобия известен в двух формах - лимонно-жел-той и белой ( точка перехода 183 С), пентахлорид тантала окрашен в белый цвет. Соляная кислота растворяет ТаСЬ на холоду, но через некоторое время раствор становится гелеобразным. Пентахлорид ниобия растворяется в концентрированных соляной и серной кислотах, при разбавлении выпадает ниобиевая кислота. [3]
Пентахлориды ниобия и тантала реагируют со спиртами, фенолами, карбоновыми кислотами и другими органическими гидро-ксилсодержащими соединениями с образованием групп - М - О - R и отщеплением хлористого водорода. Число атомов хлора, связанных с центральным атомом и способных замещаться в этих реакциях, зависит от природы реагирующих соединений и условий реакции. Так, расплавленный фенол реагирует с твердыми пентахлоридами, образуя ( Nb, Та) ( ОСвН5) в, а ( i-нафтол при кипячении с пентахлоридами, суспендированными в четыреххлористом углероде ( обратный холодильник), образует М ( ОС10Н) 5, где М Nb или Та. Но при пропускании через реакционную смесь сухого аммиака осаждается хлорид аммония и в растворе образуется пентаэтилат. Пентаметоксиниобий ( V), Nb ( OCH3) 5, ( tnn 60 С) и пентаметок-ситантал ( V), Та ( ОСН3) 5, ( tan 50 С) при комнатной температуре являются твердыми веществами. [4]
Пентахлорид ниобия - кристаллическая го цвета. [5]
Пентахлорид ниобия из испарителя через вентиль тонкой регулировки 13 подается в камеру, в которой смешивается с рабочей газовой смесью и поступает в реакционную камеру. [6]
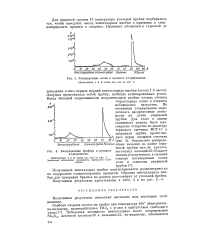 |
Распределение олова в процессе хлорирования. Обозначения А и Б такие же, как на 2.| Распределение фосфора в процессе хлорирования. [7] |
Полученный пентахлорид ниобия контролировался радиометрически на содержание соответствующих примесей. [8]
Получен пентахлорид ниобия с содержанием 0 01 % Та, 0 002 % Fe. [9]
Разделение пентахлоридов ниобия и тантала в одной колонне возможно, но невыгодно при содержаниях пентахлорида тантала в смеси 3 - 6 % от суммы хлоридов. Колонна имеет 40 реальных тарелок; объем куба 0 2 м3, диаметр 100 мм. [10]
Очистка пентахлорида ниобия может быть иллюстрирована следующим примером. Технические пентахлориды, содержавшие 34 % Nb Та, 0 35 % Ti, 0 4 % А1, 0 005 % Si, 4 5 % Fe ( остальное хлор), в количестве 225 кг загружали в куб колонны. [11]
Реакция пентахлоридов ниобия или тантала с диметилцин-ком в пентане дает золотисто-желтые кристаллы триметильных производных МезМСЬ, где М Mb или Та. Эти комплексы разлагаются при комнатной температуре и легко окисляются. [12]
Образование метилатных производных пентахлоридов ниобия и тантала было изучено количественно путем измерения рН раствора в абсолютированном метаноле. [13]
 |
Схема вакуумной дуговой электропечи. [14] |
Процесс восстановления пентахлорида ниобия водородом может быть осуществлен как непрерывный. Образующийся металлический ниобий осаждается на зернах ниобия, которые частично выводят из реактора. Получаемый металл содержит менее 0 05 % примесей. [15]
Страницы: 1 2 3 4