Передача - протон
Cтраница 1
Передача протона молекуле олефина идет также для первичных ионов легче, чем для вторичных, и для вторичных легче, чем для третичных. Наиболее энергетически выгодна передача протона в том случае, когда образующийся ион - третичный. [1]
Процесс передачи протона является обратимым. В прямой реакции молекула уксусной кислоты передает протон молекуле воды, выступающей в качестве основания. В обратной реакции кислотой является ион гидроксония Н3О, а основанием ацетат-ион. [2]
Процесс передачи протона, обусловливающий аномальную подвижность водородного иона, аналогичен прототропному обмену, который определяет скорость при катализе кислотами и основаниями. Для реакций последнего типа имеет место соотношение ( ср. [3]
Процесс передачи протона от кислоты к основанию называется протолизом, а ионно-молекулярное равновесие, устанавливающееся после передачи протона, - протолитическим или кислотно-основным. Кислоты и основания, соответственно теряющие и приобретающие протоны, называют протолитами. [4]
С реакцией передачи протона от одной молекулы или иона к другой частице связаны многие процессы, происходящие в растворах. [5]
Сама реакция передачи протона называется протолитической и выражается общей схемой АН В - А - ВН; где АН - кислота, а В - - основание. Поскольку обратный процесс также связан с передачей протона, то и продукты реакции по отношению друг к другу являются кислотой и основанием. [6]
С претерпевают передачу протона, находящегося в анионе в положении 3, к внутрисферному амину с образованием ониевого катиона и выходом его во внешнюю сферу. [7]
Поскольку при передаче протона частица кислоты отдает один положительный элементарный заряд, то в каждой сопряженной паре Кислота / Основание присутствует, как минимум, один ион, а заряд частицы кислоты на единицу больше, чем у частицы основания ( ср. [8]
Реакция заканчивается передачей протона от карбкатиона катализатору или исходному алкену; возможен также отрыв гидрид-иона от исходного алкена карбкатионом. В последнем случае образуется алкенильный ион, дальнейшие превращения которого ведут к образованию высоконенасыщенных продуктов, прочно связанных с поверхностью катализатора, или циклических углеводородов. [9]
Реакция заканчивается передачей протона от карбкатиона катализатору или исходному алкеяу; возможен также отрыв гид -, рид-иона от исходного алкена карбкатионом. В последнем случае образуется алкенильный ион, дальнейшие превращения которого ведут к образованию высоконенасыщенных продуктов, прочно связанных с поверхностью катализатора. [10]
В последнем случае передача протона происходит между кислотной и основной группами в одной молекуле. [11]
Соотношение теплот реакции передачи протона карбоний-ионом ( I) пропилену с образованием 4-метилпентена - 1 и 4-метилпентена - 2 такое же, как и при передаче протона катализатору. Реакции ( 3) и ( 4) приводят к одинаковым продуктам, и указать, какая из них реально протекает, затруднительно. Видимо, реакция ( 3) протекает с большей скоростью, так как эта реакция мономолекулярная, с высоким значением пред-экспоненты в выражении константы скорости, а реакция ( 4) - реакция второго порядка, и разница в энергиях активации их не должна быть большой. [12]
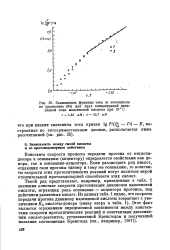 |
Зависимость функции тока от потенциала. [13] |
Константа скорости процесса передачи протона от кислоты-донора к основанию ( акцептору) определяется свойствами как донора, так и основания-акцептора. Если рассмотреть ряд кислот, отдающих свои протоны одному и тому же основанию, то константы скорости этих протолитических реакций могут являться мерой относительной протонодонорной способности этих кислот. [14]
Способности кислоты к передаче протона, а основания к присоединению протона должны выражаться в состоянии равновесия, которое устанавливается в системе, состоящей из кислоты, сопряженного с ней основания и протонов. Однако свободные протоны не могут существовать в растворе, поэтому невозможно привести абсолютную меру кислотно-основных способностей сопряженной пары кислота-основание. Если, однако, сопряженная пара кислота-основание существует в растворе определенного растворителя, то устанавливается состояние равновесия, которое можно определить экспериментально. Но оно не является исключительной мерой донорно-акцепторных свойств сопряженной пары, а характеризует реакцию между кислотой ( или основанием) и молекулами этого растворителя. [15]
Страницы: 1 2 3 4