Большинство - каталитическая реакция
Cтраница 1
Большинство каталитических реакций протекает на пористых частицах катализатора. Процессы тепло - и массообмена внутри пористой частицы и на ее поверхности часто существенным образом влияют на результирующую скорость реакции. Поэтому анализ указанных процессов имеет большое практическое значение. [1]
Большинство каталитических реакций осуществляется на пористых катализаторах, внутренняя поверхность которых состоит из пор, каналов разных размеров и длины. Эти поры могут быть изолированными или связанными друг с другом. Основным фактором, определяющим скорость и характер движения газов в порах катализатора, является размер пор. Скорость свободного движения молекул может достигать 1000 м / с, а торможение движения в порах связано с соударениями между молекулами газа и со стенками пор. [2]
Большинство каталитических реакций неизбирательны, что налагает известные ограничения на кинетические методы анализа. [3]
Большинство каталитических реакций осуществляется на пористых катализаторах, внутренняя поверхность которых состоит из пор, каналов разных размеров и длины. Эти поры могут быть изолированными или связанными друг с другом. Основным фактором, определяющим скорость и характер движения газов в порах катализатора, является размер пор. Скорость свободного движения молекул может достигать 1000 м / с, а торможение движения в порах связано с соударениями между молекулами газа и со стенками пор. [4]
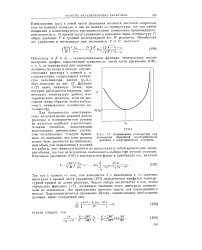 |
Оптимальная температура для. [5] |
Для большинства экзотермических каталитических реакций работа реактора в изотермическом режиме не является наиболее удовлетворительным способом, позволяющим использовать минимальное количество катализатора. [6]
Практически большинство известных каталитических реакций занимает среднее положение между этими двумя предельными случаями. [7]
 |
Изменение интенсивности полосы с v2890 см а после прекращения подачи этилена [ Dent A.L., Kokes R.J., J. Phys. Chem., 74, 3653 ( 1970 ]. [8] |
Механизмы большинства используемых каталитических реакций намного сложнее, и, чтобы все стало понятным, их необходимо тщательно4 изучить на молекулярном уровне. Однако можно надеяться, что будут разработаны практические методы расчета каталитических эффектов и механизмов каталитических реакций для реальных промышленных условий. [9]
В большинстве каталитических реакций участвуют несколько различных типов атомов и молекул. Определение механизма реакции и природы сил, действующих между этими атомами и молекулами и между ними и поверхностью, является, естественно, сложной задачей, но она может быть упрощена путем изучения адсорбционного поведения одного типа атомов или молекул. Такие исследования показали, что при адсорбции некоторых молекул на определенных адсорбентах связь в молекуле разрывается и возникают две связи с адсорбентом; при этом адсорбированная молекула переходит в два адсорбированных атома. Этот процесс представляет собой поверхностную химическую реакцию, а образовавшиеся адсорбированные атомы принято называть хемосор-бированными атомами. Если при достаточно низких температурах такая реакция не происходит и адсорбированные молекулы не распадаются на два адсорбированных атома, то такие молекулы называют физически адсорбированными. [10]
Хотелось бы отметить, что большинство каталитических реакций, особенно сложных, сопровождается, вероятно, эффектом саморегулирования. [11]
Хотелось бы отметить, что большинство каталитических реакций, особенно сложных, сопровождается, вероятно, эффектом саморегулирования. [12]
Основной недостаток состоит в том, что большинство каталитических реакций не избирательны, поэтому во избежание мешающих влияний необходимо предпринимать соответствующие предосторожности. [13]
Расхождение в числе общих и активных столкновений ( в сравнении с большинством каталитических реакций) необычно мало, что объясняется, очевидно, отсутствием необходимости озстиви-роваяной адсорбции молекул диарнлэтана внутренней поверхностью катализатора и подтверждает преимущественное влияние величины внешней поверхности катализатора. [14]
Влияние времени контактирования - г или обратной t величины объемной скорости газа, однотипно для большинства каталитических реакций. Это объясняется тем, что общее количество перерабатываемого газа при уменьшении времени пре-бывания газа в аппарате возрастает в значительно большей степени, чем снижается концентрация продукта в конечном газе. [15]
Страницы: 1 2