Большинство - ферментативная реакция
Cтраница 1
Большинство ферментативных реакций относится к бимолекулярным, вследствие чего кинетические расчеты Михаэлиса - Ментен необходимо расширить. [1]
В большинстве ферментативных реакций участвуют субстраты, молекулы которых достаточно малы по сравнению с молекулами самих ферментов. Естественно поэтому, что при образовании фермент-субстратного комплекса лишь незначительная часть пептидных связей и боковых цепей аминокислот оказывается в непосредственном контакте с молекулой субстрата. [2]
Максимальная скорость большинства ферментативных реакций включает константу скорости, отражающую изменения ковалентных связей, так что соответствующий изотопный эффект можно интерпретировать непосредственно-в терминах механизма реакции. [3]
Или субстраты: большинство ферментативных реакций проходит между молекулами субстратов, одновременно связанных на ферменте. [4]
Оптимальная температура для большинства ферментативных реакций 30 - 40 С, максимальная 55 - 60 С. При температуре 80 С ферменты инактивируются. [5]
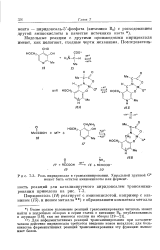 |
Роль пиридоксаля в трансаминировании. Хиральной группой G может быть остаток аминокислоты или фермент. [6] |
Для неферментативных реакций трансаминирования при каталитическом действии пиридоксаля требуется введение ионов металлов; для большинства ферментативных реакций трансаминирования эту функцию выполняет белок. [7]
Полная разработка этих проблем в значительной мере будет, вероятно, способствовать выяснению роли ионов металлов в большинстве ферментативных реакций органических фосфатов. [8]
Четыре главные особенности отличают неферментативные реакции, требующие участия пиридоксаля, от ферментативных реакций. Прежде всего для большинства ферментативных реакций не требуется иона металла, тогда как для неферментативных реакций он необходим. [9]
Из проведенного анализа следует, что стационарная скорость реакции (6.1) при [ S ] 0 [ E ] 0 должна гиперболически зависеть от. Эти закономерности действительно характеризуют кинетику большинства ферментативных реакций. [10]
Значения Ка и Кь в сравнении с Ка и Кь дают значительную информацию при рассмотрении пути, по которому ионизирующие группы активного центра взаимодействуют с субстратом. К сожалению, даже сложная схема реакции, приведенная выше, вероятно, является слишком простой для большинства ферментативных реакций, и для них должны быть предложены еще более сложные схемы. [11]
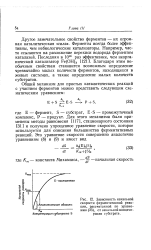 |
Зависимость начальной скорости ферментативной реакции, рассчитанной по уравнению ( 33, от начальной концентрации субстрата. [12] |
Для этого механизма были применены методы равновесия [117], стационарного состояния [31 ] и получено упрощенное уравнение скорости, которое используется для описания большинства ферментативных реакций. [13]
Применяя мультиллетную теорию, возможно систематизировать [540, 541] как реакции ферментативного катализа, так и реакции, катализируемые химическими моделями ферментов. В дальнейшем [542] этой систематикой охвачены все известные ферменты. Большинство ферментативных реакций имеет дублетный или триплетный индекс, причем разным типам ферментов, большей частью соответствуют разные индексы реакций. [14]
Четыре особенности отличают ферменты от всех прочих катализаторов. Во-первых, эти биокатализаторы исключительно эффективны. При оптимальных условиях большинство ферментативных реакций протекает в 108 - 1011 раз быстрее, чем те же реакции в отсутствие ферментов. Следует при этом иметь в виду, что скорость отдельных стадий ферментативных реакций лимитируется диффузией реагирующих веществ или, во всяком случае, зависит от нее. Таким образом, многие химические реакции, которые обычно протекают только при высоких температурах или только в сильно кислой или сильно щелочной среде, в присутствии соответствующих ферментов могут идти быстро и количественно при комнатной температуре и при значениях рН, близких к нейтральному. Во-вторых, для большинства ферментативных реакций характерна высокая специфичность как в отношении природы катализируемой реакции, так и в отношении структуры используемого субстрата. В-третьих, круг реакций, катализируемых ферментами, необычайно широк. Ферменты катализируют реакции гидролиза, поликонденсации, окисления - восстановления, дегидрирования, альдольной конденсации, реакции переноса различных групп, а также ряд других реакций. [15]
Страницы: 1 2