Большинство - органическая реакция
Cтраница 1
Большинство органических реакций включает несколько последовательных ( элементарных) стадий. Детальное описание совокупности этих стадий называется механизмом. [1]
Большинство органических реакций подвержено различного рода каталитическим воздействиям, и почти каждое химическое соединение ( или смесь соединений) способно в той или иной мере катализировать определенную реакцию. В целях ограничения круга предлагаемых вопросов в настоящем разделе в качестве катализаторов рассматриваются только вещества, способные обеспечить желаемый практический результат, который не может быть обычно достигнут в отсутствие катализатора. [2]
Большинство органических реакций протекает в жидкой среде и влияние молекул растворителя на реакцию может варьироваться в широких пределах - от инертной среды для реагирующих молекул, до непосредственного и отнюдь не второстепенного участника различных элементарных актов. Отметим лишь, что в большинстве своем они основываются на классических электростатических представлениях. [3]
Большинство органических реакций происходит между молекулами, между молекулами и ионами либо между молекулами и свободными радикалами. [4]
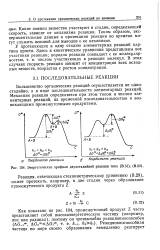 |
Энергетические профили двухстадийной реакции типа ( В. 31, ( В. 32. [5] |
Большинство органических реакций осуществляется не одностадийно, а в виде последовательности элементарных реакций. Механизм реакции определяется при этом типом и числом элементарных реакций, их временной последовательностью и возникающими промежуточными продуктами. [6]
Большинство органических реакций состоят более чем из одной стадии. Поэтому необходимо рассмотреть кинетические выражения, которые вытекают из некоторых наиболее важных случаев многостадийных реакций. Стадии, определяющей скорость реакции, может предшествовать быстрое равновесие. [7]
Большинство органических реакций, рассматриваемых в этой книге, являются ионными, хотя в гл. Такое деление дает несколько больше сведений о механизме реакций, однако в некоторых случаях невозможно сразу классифицировать реакцию как гемолитическую или гетеролитическую. [8]
Большинство органических реакций протекает по гетеролитическому механизму. [9]
Большинство органических реакций проводят с молекулами, находящимися в основном электронном состоянии. Специальную область составляют фотохимические реакции [1], при которых реагирующие молекулы предварительно облучают светом, переводя их в электронно-возбужденное состояние. Молекула не может находиться в возбужденном состоянии долгое время, она должна потерять избыточную энергию тем или иным способом. Однако химическая реакция является не единственным способом высвобождения дополнительной энергии. В данной главе сначала рассматриваются электронно-возбужденные состояния и процессы, приводящие к переходу в такие состояния. Затем обсуждаются возможные пути превращения возбужденных молекул, в первую очередь физические, а потом химические. С фотохимией тесно связана электронная спектроскопия. [10]
Большинство органических реакций в отличие от неорганических является необратимыми. Следовательно, закон действующих масс к ним неприменим, и они, естественно, не имеют таких характеристик, как константы равновесия. [11]
Однако большинство органических реакций и некоторые неорганические не являются стехиометрическими; такие реакции часто идут одновременно в нескольких направлениях. [12]
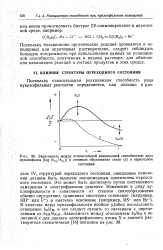 |
Зависимость между Относительной реакционной способностью двух нуклеофилов [ log ( feNJ & Nz ] и степенью образования связи ( г в переходном. [13] |
Поскольку большинство органических реакций проводится в неполярных или апротонных растворителях, следует соблюдать большую осторожность при использовании данных по реакционной способности, полученных в водном растворе, для объяснения механизмов реакций и состава продуктов в этих средах. [14]
Для большинства органических реакций указанное превышение достаточно велико, и потому, с точностью порядка 0 5 ккал / моль, АЕ и высоту барьера для бимолекулярных реакций можно считать совпадающими. [15]
Страницы: 1 2 3 4