Большинство - органическая реакция
Cтраница 3
Барботажные реакторы особенно пригодны для осуществления реакций, протекающих в кинетической области, что характерно для большинства органических реакций. Вместе с тем равномерное распределение газа по сечению аппарата обеспечивает достаточно развитую поверхность контакта между фазами, а непрерывный барботаж газа через слой катализатора - пере-мешивание его. [31]
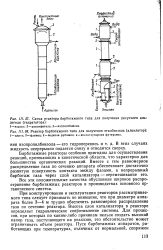 |
Схема реактора барботажного типа для получения уксусного альдегида ( гидрататора. / - корпус. 2-расширитель. 3-каплеотбойиик. [32] |
Барботажные реакторы особенно пригодны для осуществления реакций, протекающих в кинетической области, что характерно для большинства органических реакций. Вместе с тем равномерное распределение газа по сечению аппарата обеспечивает достаточно развитую поверхность контакта между фазами, а непрерывный барботаж газа через слой катализатора - перемешивание его. [33]
Наконец, в пользу рассмотренного выше ионного механизма реакции азосочетания свидетельствует то, что в отличие от большинства органических реакций она идет с высокой скоростью даже на холоду, что в основном свойственно ионным реакциям. [34]
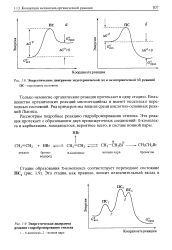 |
Энергетическая диаграмма реакции гидробромирования этилена. [35] |
Только немногие органические реакции протекают в одну стадию. Большинство органических реакций многостадийны и имеют несколько переходных состояний. [36]
 |
Схема электронного состояния.| Схема электронного состояния.. б - ок.| Схема электронного состояния. а - атома фтора. б - двухвалентного фторкатиона. в - иона ( аниона фтора. [37] |
Большинство органических реакций происходит между молекулами, между молекулами и ионами либо между молекулами и свободными радикалами. [38]
 |
Схема электронных состояний.| Схема электронных состояний. я - атома фтора, б - двухвалентного фторкатиона в - аниона фтора. [39] |
Большинство органических реакций происходит между молекулами, между молекулами и ионами, либо между молекулами и свободными радикалами. [40]
Большинство органических реакций происходит между молекулами, между молекулами и ионами либо между молекулами и свободными радикалами. [41]
Последующие главы йудут посвящены главным образом описанию конкретных органических реакций - Развитие практического понимание органической химии требует совершенного овладения определеннымЕ фундаментальными типами реакций, которые лежат в основе широкого разнообразия индивидуальных реакций. Большинство органических реакций протекает в несколько Стадий; эти стадии составляют механизм реакции. Знание детальных механизмов реакций часто вскрывает близкое родство реакций, которые в других отношениях могут казаться несходными. В настоящей главе будут обсуждаться методы проведения исследований органических реакций с целью определения их механизмов, В главе рассматриваются типы экспериментальных исследовании, которые поставляют исходные данные, в методы, которыми из таких данных можно извлекать информацию о механизмах реакций. [42]
На практике реализовать идеальные условия не удается вследствие разнообразия природы органических молекул и их. Большинство органических реакций протекает с малой скоростью, а потому для увеличения скорости реакции часто приходится применять нагревание и катализаторы. Более того, хотя - в литературе имеются лишь очень ограниченные сведения по константам равновесия органических реакций, громадный объем препаративных данных показывает, что равновесный выход целевых продуктов для большинства органических процессов редко приближается к 100 %, даже если подбор концентраций реагентов и условий реакции способствует максимальному смещению равновесия вправо. В конечном счете правильный выбор реагентов и условий анализа может быть сделан лишь после обсуждения скорости, равновесия и прочих факторов, влияющих на все ожидаемые взаимодействия. [43]
Отрицательно заряженные ионы, например 1 -, СНзСОО -, стремятся отдать электроны или взаимодействовать с такими частями молекул, которые несут положительный заряд, поэтому они называются электронодонорными или нуклеофильными. Большинство органических реакций протекает по гетеролитическому механизму. [44]
Количество тепла, выделяющееся или поглощающееся в ходе процесса, происходящего при постоянном объеме ( подобно описанному здесь для случая сожжения углеводорода в закрытом сосуде), отличается от количества тепла, выделяющегося или поглощающегося в случае процесса, проходящего при постоянном давлении. Поскольку большинство органических реакций проводится при постоянном давлении, теплота реакции ДЯ обычно определяется как количество тепла, выделяющееся или поглощающееся при постоянном давлении. [45]
Страницы: 1 2 3 4