Большинство - простое вещество
Cтраница 1
Большинство простых веществ и химических соединений в жидком состоянии при температуре плавления имеют незначительную вязкость. [1]
Большинство простых веществ существует в нескольких аллотропных модификациях. [2]
Большинство простых веществ является типичными металлами. У ряда элементов металлическими свойствами обладают лишь некоторые их модификации. К металлам относятся элементы главных подгрунп первых четырех групп периодической системы, все элементы с внешними d - и / - оболочками электронов. Несколько модификаций, как с металлическими, так и с неметаллическими свойствами, образуют, например, С, Р, As, Sb, Se. Устойчивость отдельных модификаций сильно зависит от внешних условий. В последнее время подробно исследовано влияние давления на фазовые превращения. [3]
Большинство простых веществ существует не в виде молекул, а представляет собой более сложные макроскопические образования с немолекулярной структурой. Характерной особенностью этого состояния является агрегация большого числа атомов ( порядка постоянной Авогадро) в едином ансамбле, в результате чего и возникают новые свойства, о которых нельзя говорить применительно к молекулам. В силу насыщенности ковалентной связи в молекуле I fa2 ( r) и отсутствия межмолекулярного взаимодействия натрий в парообразном состоянии обладает диамагнетизмом ( в отличие от одноатомного пара) и является диэлектриком. [4]
Большинство простых веществ существует не в виде молекул, а представляет собой более сложные макроскопические образования с немолекулярной структурой. Характерной особенностью этого состояния является агрегация большого числа атомов ( порядка постоянной Авогадро) в едином ансамбле, в результате чего и возникают новые свойства, о которых нельзя говорить применительно к молекулам. В силу насыщенности ковалентной связи в молекуле Na2 ( г) и отсутствия межмолекулярного взаимодействия натрий в парообразном состоянии обладает диамагнетизмом ( в отличие от одноатомного пара) и является диэлектриком. [5]
Большинство простых веществ могут существовать в одном из трех агрегатных состояний-газообразном, жидком или твердом. Мы уже познакомились с газовым состоянием, выяснили строение газов и узнали, каким законам они подчиняются; все это привело нас к выводу о наличии в газах слабых сил межмолекулярного взаимодействия, называемых вандерваальсовы-ми силами. Затем мы установили, что для твердого состояния характерно наличие высокой упорядоченности; здесь мы также столкнулись с межмолекулярными силами, которые существуют в металлах, ионных кристаллах и молекулярных веществах. Теперь настало время обратиться к жидкому состоянию, изучение которого дает еще больше сведений о межмолекулярных силах. [6]
Большинство простых веществ существует не в виде молекул, а представляет собой более сложные макроскопические образования с немолекулярной структурой. Характерной особенностью этого состояния является агрегация большого числа атомов ( порядка постоянной Авогадро) в едином ансамбле, в результате чего и возникают новые свойства, о которых нельзя говорить применительно к молекулам. В силу насыщенности ковалентной связи в молекуле Na2 ( г) и отсутствия межмолекулярного взаимодействия натрий в парообразном состоянии обладает диамагнетизмом ( в отличие от одноатомного пара) и является диэлектриком. [7]
В большинстве простых веществ все атомы образуют одну правильную систему точек. Однако у а - и 3-марганца атомы распределяются по нескольким правильным системам и, следовательно, кри-сталлохимически различны. [8]
Исключительно активно протекает взаимодействие фтора с большинством простых веществ. [9]
Исключительно активно протекает взаимодействие фтора с большинством простых веществ. [10]
Фосфор химически активен и непосредственно взаимодействует с большинством простых веществ. [11]
Наиболее важным химическим свойством кислорода является его способность соединяться с большинством простых веществ с выделением теплоты и света. [12]
Кислород обладает высокой химической активностью, особенно при нагревании и в присутствии катализатора; с большинством простых веществ он взаимодействует непосредственно, образуя оксиды; лишь по отношению к фтору проявляет восстановительные свойства. [13]
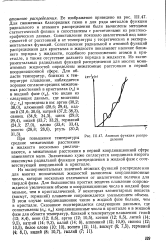 |
Атомная функция распределения. [14] |
Из экспериментальных значений атомных функций распределения для многих моноатомных жидкостей вычислены координационные числа, которые несколько отличаются от аналогичных величин для твердой фазы. Для большинства простых веществ плавление сопровождается увеличением объема и координационные числа в жидкой фазе меньше, чем в кристаллической, У некоторых элементарных веществ ( висмут, германий) плавление сопровождается уменьшением объема. [15]
Страницы: 1 2 3