Большинство - соединение
Cтраница 2
Большинство соединений канцерогенно для всех видов животных, включая человекообразных обезьян. Нитрозометилуретан раздражает органы дыхания ( возможен отек легких за счет образования NOz); поражает конъюнктиву; кожные высыпания появляются даже от действия паров. [16]
Большинство соединений, обычно используемых в качестве восстановителей ( например, тексилборан, дисиамилборан, 9 - ББН), существует в виде димеров. Другие производные трехвалентного бора, как правило, являются мономерами. [17]
Большинство соединений получено впервые. Строение подтверждается превращением их в известные фенацетины и ИК-спектрами. [18]
Большинство соединений, обычно используемых в качестве восстановителей ( например, тексилборан, дисиамилборан, 9 - ББН), существует в виде димеров. Другие производные трехвалентного бора, как правило, являются мономерами. [19]
Большинство соединений имеет форму квадратной антипризмы. Однако, согласно спектральным данным ( ИК-спектры и спектры КР), в растворе ион Mo ( CN) 8 - 4 имеет структуру квадратной антипризмы. [20]
Большинство соединений растворяется после трехминутного перемешивания; исключение составляет тетраметиламмонийиодид, для растворения которого необходимо примерно 15-минутное перемешивание. Кокаингидрохлорид имеет высокий эквивалентный вес, поэтому вес образцов этого вещества составлял 70 - 100 мкг. [21]
Большинство соединений имеет отрицательную теплоту образования. [22]
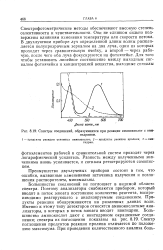 |
Спектры соединений, образующихся при реакции аминокислот с нин. [23] |
Большинство соединений не поглощает в видимой области спектра. Поэтому анализаторы снабжаются прибором, который вводит в поток элюата постоянное количество реагента, воспроизводимо реагирующего с анализируемым соединением. Продукты реакции обнаруживаются на различных длинах волн. Именно к этому типу детекторов относятся аминокислотные анализаторы, в которых в поток элюата вводят нингидрин. Большинство аминокислот дают с нингидрином окрашенные соединения; спектры их поглощения показаны на рис. 8.19. Спектр поглощения продуктов реакции пролина отличается по положению максимума. [24]
 |
Подвижности ионов в метаноле и этаноле. [25] |
Большинство соединений, проявляющих кислотные свойства в воде, в спиртовых растворах также ведут себя как кислоты, поэтому спиртах выполнимы различные реакции нейтрализации, которые можно изучать препаративно, кондуктометрическим или потенцио-метрическим титрованием или с помощью обычных цветных индикаторов. [26]
Большинство соединений, растворимых в серной кислоте, ведут себя как электролиты, так как их основные свойства достаточны, чтобы образовать сильные водородные связи с серной кислотой, и, по-видимому, в направлении этих связей осуществляется перенос протона, что приводит к ионизации. Высокая диэлектрическая проницаемость растворителя способствует довольно полной диссоциации ионизированных соединений. Основания образуют в серной кислоте бисульфат-ион HSOJ, и благодаря низкому сродству к протону серной кислоты они, по-видимому, являются в этом растворителе самым обширным классом электролитов. Многие вещества, не проявляющие основных свойств в воде, в серной кислоте ведут себя как основания. Серная кислота оказывает нивелирующее действие на силу оснований так же, как жидкий аммиак на силу кислот. [27]
Большинство соединений принадлежит к 5 ] 3-ряду, ОН-группа в положении 3 также имеет ( за одним исключением) - конфигурацию. Физиологически активные соединения содержат гидроксил в положении 14 3; в то же время группы ОН и СО в положениях 11, 12, 16 и 19, по-видимому, оказывают меньшее влияние на активность. [28]
Большинство соединений, которые могут привести к подавлению сцинтилляции, при перегонке остаются в осадке вместе с радиоактивным иодом ( если он имеется) и бикарбонатом. Серьезные помехи определенно создают источники люминесценции в лаборатории. [29]
Большинство соединений, применяемых в качестве антиоксидан-тов, такие, как одноатомные фенолы и амины, необратимо переходят в окисленные формы, поэтому для таких систем отсутствует окислительно-восстановительный потенциал. Однако специальные методические приемы позволяют и в данном случае охарактеризовать восстановительные свойства веществ. Превращение фенолов в окислительно-восстановительных реакциях осуществляется в двух стадиях: обратимая реакция с образованием феноксильных радикалов и последующий медленный и необратимый переход в стабильные конечные продукты. [30]
Страницы: 1 2 3 4