Большинство - хлорид
Cтраница 2
Большинство хлоридов металлов хорошо растворимо в воде. Исключения составляют: AgCl, Hg2Cl2l T1C1, PbClj, в холодной воде они очень мало растворимы. [16]
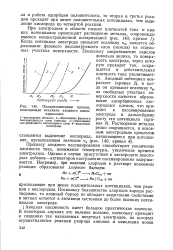 |
Поляризационные кривые, поясняющие механизм анодного пассивирования. [17] |
Поскольку большинство хлоридов хорошо растворимы, то хлорный барьер не обладает защитными свойствами и металл остается в активном состоянии до более высоких потенциалов электрода. [18]
Поскольку большинство хлоридов легко возгоняется, нагревание следует начинать с низкой температуры и постепенно повышать ее. [19]
Поскольку большинство хлоридов легко возгоняется, нагревание следует начинать с низкой температуры и постепенно повышать. [20]
Следовательно, большинство хлорида кальция содержится в тяжелой смоле, богатой механическими примесями. [21]
Известно, что большинство хлоридов, введенных в бетон при затворении, в той или иной мере ускоряет твердение. [22]
Этому условию удовлетворяет большинство хлоридов металлов. С другой стороны, многие окислы металлов: А12О3, BeO, CaO, La2O3, MgO, MnO, SrO, ThO2, ZrO2, HfO2, образующие капли расплава при введении в пламя растворов сернокислых или азотнокислых солей этих металлов, имеют недостаточную для полного испарения упругость паров. Вследствие неполного испарения вводимого в пламя вещества результаты определения концентрации какого-либо элемента, содержащегося в этом веществе, оказываются заниженными. Этот тип влияния посторонних элементов на результаты анализа в пламенах ( как при эмиссионных, так и при абсорбционных измерениях) встречается чаще всего. [23]
Вследствие ковалентности связи большинство хлоридов тугоплавких металлов слабо проводят электричество. Кроме того, сравнительно низкая температура кипения ( или возгонки) определяет высокое давление пара хлоридов при температуре электролиза. Поэтому электролиз расплавов чистых хлоридов тугоплавких металлов практически невозможен. Электролиз ведут из их смеси с К. При этом образуются химические соединения, понижающие давление пара хлоридов над расплавом. Обычно в электролите концентра цию хлоридов тугоплавких металлов поддерживают 3 - 12 мол. Концентрация хлоридов тугоплавких металлов должна быть достаточной, чтобы не допустить возникновения концентрационной поляризации на катоде, что может вызвать разряд посторонних ионов, снизить выход по току и чистоту получаемого металла. [24]
Вследствие ковалентности связи большинство хлоридов тугоплавких металлов слабо проводят электричество Кроме того, сравнительно низкая температура кипения ( или возгон ки) определяет высокое давление пара хлоридов при темпера туре электролиза Поэтому электролиз расплавов чистых хло РИДОВ тугоплавких металлов практически невозможен Элек тролиз ведут из их смеси с К. [25]
В нейтральных растворах большинства хлоридов, бромидов и йоди-дов титаи стоек при любых концентрациях, вплоть до температуры кипения, и в отличие от кислотостойких сталей не подвергается точечной коррозии. [26]
С), к которым относится большинство хлоридов, можно ожидать снижения емкости сорбента в условиях повышенных температур. Недостатком метода является необходимость подогрева и тер мостят ирования колонны и соединении во избежание конденсации ларов. [27]
Он является хорошим растворителем для 80s н большинства хлоридов многовалентных металлов. Взаимодействие подобных растворов может служить удобным методом получения соответствующих безводных сульфатов. [28]
Он является хорошим растворителем для 80s и большинства хлоридов многовалентных металлов. Взаимодействие подобных растворов может служить удобным методом получения соответствующих безводных сульфатов. [29]
Он является хорошим растворителем для 80s и большинства хлоридов многовалентных металлов. [30]
Страницы: 1 2 3 4