Большинство - цеолит
Cтраница 2
Легкость, с которой происходит обмен между катионами кристаллов цеолита с катионами окружающего их водного раствора, является характерной особенностью большинства цеолитов. Изменение молекулярно-сите-вых свойств определяется как размером и типом катионов, так и расположением их относительно полостей. Замена одного катиона другим влияет не только на молекулярно-ситевые свойства, но и на термическую стабильность цеолитов. Наиболее термически стоек кальциевый цеолит, активность его резко падает лишь при температуре выше 800 С. [16]
Молекулы СО2 достаточно малы - их диаметр составляет около 0 31 нмк ( 3 1 А), что позволяет им проникать во внутреннюю структуру большинства цеолитов. [17]
Кумбс [17] пришел к выводу, что анальцим, вайракит, морденит, гейландит и ломонтит так часто встречаются в ассоциации с другими минералами в системе CaO - Al2O3 - ( MgJFe) O - SiO2 - H2O потому, что для каждого цеолита существует предел термодинамической стабильности или, по крайней мере, устойчивой метастабильности. Большинство цеолитов термодинамически нестабильны, но, к счастью, их превращение в более стабильные цеолиты происходит, обычно очень медленно, на что указывает длительное существование природных цеолитов. В первом приближении можно сказать, что природные цеолиты обычно содержат меньше воды, чем синтетические, и превращение их обычно приводит к образованию модификаций с меньшим содержанием воды. [18]
В табл. 8.18 - 8.23 приведены некоторые величины изостери-ческих теплот адсорбции и показано, как они изменяются с увеличением количества адсорбированного вещества. Для большинства цеолитов изостерические теплоты даны для двух катионных форм при малых, близких к нулевым, и высоких степенях заполнения адсорбатом. Приведенные данные позволяют судить о степени однородности внутренней поверхности по отношению к данному адсорбату. [19]
Третья проблема связана с локализацией атомов Si и А1 в тет-раэдрических положениях. Однако для большинства цеолитов рентгеноструктурные и другие данные указывают на совершенно беспорядочное распределение этих атомов по каркасу. Следует отметить, что можно не обратить внимание на дальний порядок, если при рентгеноструктурном анализе предположить пространственную группу со слишком высокой симметрией. Такая пространственная группа предполагает упорядоченное расположение атомов алюминия. [20]
Указанные особенности поведения окиси алюминия приводят ж тому, что в алюмосиликатах он может способствовать образованию минеральных веществ с ионной каркасной структурой или жесткой структурой с открытыми или закрытыми каналами. Такую структуру имеет большинство цеолитов, содержащих структурную воду. Эта вода может находиться в кристаллах в переменном количестве в виде отдельных молекул, не связанных или слабо связанных электростатическими силами - с ионами кристаллического вещества. [21]
В табл. 2.4 для большинства цеолитов даны величины свободного объема ( см3 / см3) или доли свободного объема Vf. [22]
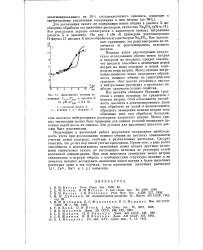 |
Зависимость степени замещения та / -. а В Цеолите X от рН ( CNa 0 1 N. [23] |
Все цеолиты обладают большим сродством к ионам водорода по сравнению с ионами натрия. Этим объясняется способность цеолитов к декатионированию даже при обработке их водой и невозможность обратного замещения ионами натрия всех обменных мест при обработке большинства цеолитов нейтральными растворами хлористого натрия. Метод кривых титрования может быть применен для оценки условий отмывания цеолитов водой после их синтеза. Эти условия для различных цеолитов должны быть различными. [24]
Проблема установления связи между теплотой адсорбции газов и паров цеолитами и их внутренним строением и химическим составом - одна из центральных в фи-зико-химии молекулярных сит. В ранних работах, когда объектами исследований являлись природные цеолиты, всякие попытки соотнесения величин теплот адсорбции с какими-либо конкретными адсорбционными центрами были невозможны, так как структуры большинства цеолитов были не расшифрованы, а химический состав образцов обычно не определялся. [25]
Превращения такого типа обычно связаны с продолжительностью эксперимента, и, следовательно, должны быть изучены во времени при постоянных температуре и давлении. Приведенные графики скорее отражают кинетику, чем термодинамику процесса, и их нельзя рассматривать как диаграммы фазового равновесия, поскольку не все границы полей кристаллизации нанесены. Большинство цеолитов не превращаются в продукты того же химического состава, что и исходные вещества. Поскольку опыты проводятся с избытком воды, в автоклаве может происходить селективное растворение отдельных компонентов исходного цеолита. Например, синтетический цеолит NaA превращается в цеолит анальцимного типа, содержащий меньшие количества А1203 и Na20, что указывает на преимущественное растворение этих компонентов. Цеолит NaA стабилен при 220 С в течение суток, но при более длительном нагревании превращается в цеолит Р, который в свою очередь переходит, наконец, в фазу анальцимного типа. Напротив, СаА превращается в сколецит и после этого в полевой пшат анортит-ного типа. [26]
Цеолиты широко используются в промышленности как молекулярные сита. Цеолит типа А, разработанный фирмой Union Carbide, оказался особенно удачным в этом отношении, так как эффективный размер его пор можно легко менять с помощью ионного обмена. Эффективным размерам пор большинства алюмосиликатных цеолитов посвящено много работ, но лишь в немногих из них обсуждаются способы изменения этих размеров. [27]
 |
Структура цеолитов. [28] |
Адсорбционные свойства цеолитов проявляются после их обезвоживания, так как в процессе синтеза полости кристаллов заполняются молекулами воды. Она может быть удалена из кристаллов при нагревании до 300 - - 350 С. При этом решетка - большинства цеолитов сохраняе - j свою структуру. После дегидратации цеолиты обладают высокой адсорбционной емкостью. Объем пустот в них может составить до 50 % общего объема кристаллов. Важной особенностью решетки цеолита является высокая термостабильность. Так, цеолит NaA устойчив до 650 С, NaY - до 700 - 750 С, CaY - до 800 С, LaY - до 850 С. [29]
Титов говорят об их ориентации относительно алюмосиликатного остова), имеет значение также своеобразная структура алюмосиликатного остова этих соединений. Как видно из рентгенограмм, тетраэдры Si04 и А104 в них расположены в виде колец, нанизанных одно на другое так, что образуются сквозные трубки, проходящие по всему кристаллу. В пермутитах и в большинстве цеолитов одна часть воды связана прочнее, чем другая. Аналогичные отношения имеются у других цеолитов, а также у пермутитов. [30]
Страницы: 1 2 3