3-оксипиридин
Cтраница 1
Нитрование 3-оксипиридина сопровождается окислительным расщеплением цикла и только в мягких условиях [18] ( ср. По данным Плазека [19], продукт монозамещения представляет собою 2-нитро - З - оксипиридин; продуктом дизамещения, повидимому, является 2 6-динитро - З - оксипиридин. [1]
В противоположность этому 3-оксипиридин подобен фенолу; однако оксиформа преобладает только в растворителях с низкой диэлектрической проницаемостью. [2]
С другой стороны, 3-оксипиридин, как и следовало ожидать, обладает типичной структурой фенола и проявляет свойства фенола, ограниченные, конечно, влиянием, которое оказывает на него наличие пиридинового ядра. Он дает пурпурную окраску с хлорным железом, конденсируется с формальдегидом, вступает в реакцию Манниха и легко галогенируется. Спектры поглощения в ультрафиолете для 3-окси - и 3-метоксипиридина в нейтральных и кислых растворах [82] почти идентичны ( рис. 4); в щелочных растворах спектр 3-оксипиридина значительно отличается от спектра 3-метоксипиридина, но аналогичен спектру фенола. [3]
С другой стороны, 3-оксипиридин CXXVI показывает в нейтральной среде обычный спектр и, кроме того, при переходе в щелочную область обнаруживает типичный фенольный сдвиг. [4]
Итак, при нитровании 3-оксипиридина, а равно и при его сульфировании и иодировании предпочтительно имеет место op / no - замещение. Это находится в согласии с общеизвестным фактом, что фенол при нитровании образует 30 - 40 % о-нитрофенола и лишь 14 % пара-изомера. [5]
Как видно, производные 3-оксипиридина отличаются друг от друга природой замещающей группы в положении 4 пиридинового ядра. Витамин В6 хорошо растворим в воде и этаноле. Водные растворы весьма устойчивы по отношению к кислотам и щелочам, однако они чувствительны к влиянию света в нейтральной зоне рН среды. [6]
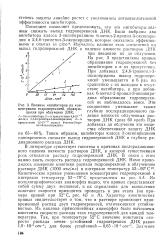 |
Влияние ингибиторов на концентрацию гидроперекисей, образующихся при облучении ДНК. [7] |
Таким образом, ингибиторы класса 3-оксипиридинов одновременно снижают выход гидроперекисей ДНК. [8]
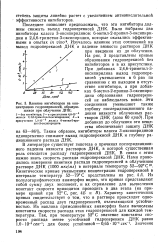 |
Влияние ингибиторов на кон - соединения уменьшают также центрацию гидроперекисей, образую - J. [9] |
Таким образом, ингибиторы класса 3-оксипиридинов одновременно снижают выход гидроперекисей ДНК и глубину радиационного распада ДНК. [10]
Получите из пиридина а - и ( 3-оксипиридины и а - и р-аминопиридины. Укажите, для каких из этих соединений возможна таутомерия. [11]
Например, в то время как алкилиро-вание солей 3-оксипиридина приводит к соответствующему эфиру, из солей щелочных металлов 2 - и 4-пиридонов при алкилировании образуются преимущественно N-алкилпроизводные. [12]
Оксипиридины обладают свойствами, характерно отличающими их от 3-оксипиридинов. [13]
Например, в то время как алкилиро-вание солей 3-оксипиридина приводит к соответствующему эфиру, из солей щелочных металлов 2 - и 4-пиридонов при алкилировании образуются преимущественно N-алкилпроизводные. [14]
Плазек [25-27], исследовавший нитрование, сульфирование и иодирование 3-оксипиридина, показал, что во всех этих реакциях имеет место преимущественно opmo - замещение. [15]
Страницы: 1 2 3