Образующаяся перекись - водород
Cтраница 3
С этой целью проведем следующий расчет для случая, когда водный раствор NaOH, co - держащий окись цинка ( 2 г на 100 мл раствора), подвергался облучению в течение 15 мин. Концентрация образующейся перекиси водорода в отсутствие окиси цинка ( за 15 мин. [31]
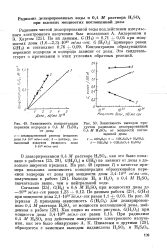 |
Зависимость концентрации.| Зависимость выходов про. [32] |
Радиолиз чистой дезаэрированнои воды под действием импульсного электронного излучения был исследован А. Концентрация образующихся перекиси водорода и водорода зависит от дозы. Это свидетельствует о протекании в этих условиях обратных реакций. [33]
Результаты опытов с 2-этилантрагидрохиноном, тетрагидро-2 - этилантрагидрохиноном и смесью ( 1: 1) обоих ( рабочая смесь) представлены в таблице. Как видно из таблицы, кислород образующейся перекиси водорода происходит целиком из элементарного кислорода, примененного для окисления, без участия кислорода гидро-ксильных групп антрагидрохинона или спирта. [34]
На рис. 3 455 показано влияние малых количеств соляной кислоты па скорость взаимодействия перекиси бария с 20 % - ной серной кислотой. Скорость выражается количеством псрманга-пата, израсходованного на титрование образующейся перекиси водорода. Количество соляной кислоты выражено п процентах по отношению к стехиометричсскому, требуемому для полного превращения перекиси бария в хлористый барий. Из рис. 3 лидио, что процесс образования Н20а заканчивается уже через / и часа при содержании соляной кислоты от 3 до 4 %, тогда как при 2 % НС1 он длится G часов. [35]
На этих реакциях основан промышленный метод получения перекиси водорода ( стр. В ходе реакции равновесие постоянно смещается вправо благодаря непрерывной отгонке из смеси образующейся перекиси водорода. [36]
 |
Окисление этилового спирта на платиновом аноде. [37] |
Действие катализаторов в процессах электроокисления может проявляться по-разному. Так, например, анионы галоидов, цианиды, роданиды и др. способствуют стабилизации промежуточно образующейся перекиси водорода и тем благоприятствуют процессу окисления, происходящему при ее участии. Введение ионов тяжелых металлов, катализирующих распад пе-рекисных соединений, оказывает обычно противоположное действие. В других случаях небольшие добавки некоторых веществ вызывают повышение потенциала анода и тем оказывают благоприятное влияние на процесс окисления. Так действуют, например, фториды, роданиды и некоторые Другие соединения, в частности, содержащие серу и азот. Детальный механизм действия этих добавок неясен; возможно, они стабилизируют нестойкие поверхностные окислы, образующиеся на аноде и этим повышают анодную поляризацию. [38]
Чтобы энзиматическое деаминирование было возможно, атакуемая аминокислота должна иметь атом водорода и амино-группу при а-углеродном атоме. Чтобы довести реакцию до конца, необходим большой избыток энзима и достаточное количество каталазы, чтобы разрушить образующуюся перекись водорода. Когда эти реакции закончатся, к реакционной смеси добавляют основание, более сильное, чем аммиак, но не способное гидролизовать возможно присутствующие аминосоединения. [39]
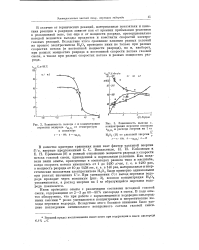 |
Зависимость выхода а. и концентрации.| Зависимость выхода а, концентрации перекиси водорода сн 0 и расхода энергии на 1 кг. [40] |
В качестве критерия сравнения нами взят фактор удельной энергии U / v, впервые предложенный С. С. Васильевым, Н. И. Кобозевым и Е. Н. Ереминым [8] и равный отношению мощности разряда к скорости потока газовой смеси, приведенной к нормальным условиям. При уменьшении U / v выход перекиси водорода проходит через максимум ( рис. 3), весовая концентрация Н202 увеличивается, а расход энергии на 1 кг образующейся перекиси водорода понижается. [41]
Исходным сырьем для производства перекиси водорода служат надсерная кислота или персульфат аммония, полученные электролизом растворов серной кислоты и сульфата аммония. Раствор надсерной кислоты или кислый раствор персульфата аммония подвергают гидролизу при повышенной температуре. Образующаяся перекись водорода отгоняется под вакуумом с парами воды и конденсируется. [42]
Исходным сырьем для производства перекиси водорода служит надсерная кислота или персульфат аммония, полученные электролизом растворов серной кислоты и сульфата аммония. Раствор надсерной кислоты или кислый раствор персульфата аммония подвергают гидролизу при повышенной температуре. Образующаяся перекись водорода отгоняется под вакуумом с парами воды и конденсируется. [43]
Не следует предполагать, что механизм с участием возбужденного НО будет иметь существенное значение при давлениях, превышающих второй взрывной предел, где приобретают большую вероятность тройные столкновения. Приведенной выше гипотезой объясняется большая часть наблюдений, сделанных при низких давлениях; увеличение диаметра трубки вызывает увеличение времени, необходимого для того, чтобы молекулы перекиси водорода достигли стенки, и, таким образом, снижает вероятность стабилизации молекул перекиси водорода; вместе с тем снижается и вероятность рекомбинации гидроксилов на стенке. Остается неясным, почему тетраэтилсвинец повышает количество образующейся перекиси водорода, как это установлено Танкером. Возможно, что тетраэтилсвинец селективно забирает атомарный водород, обладающий относительно высокой скоростью движения и, как это показал Гейб [20], особенно быстро разлагающий перекись водорода. [44]
Как видно из сопоставления величин стандартных потенциалов, наиболее отрицательным потенциалом обладает реакция образования перекиси водорода. Следовательно реакция ( 27) может протекать лишь в том случае, если перенапряжение реакции ( 30) велико. Реакция ( 29) тоже должна быть в максимальной степени заторможена, ибо в противном случае вся образующаяся перекись водорода будет успевать восстанавливаться до воды. [45]
Страницы: 1 2 3 4