Перекрывание - зона
Cтраница 1
 |
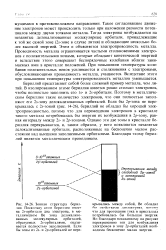
Зонная структура металла. [1] |
Перекрывание зон объясняет металлические свойства, например, щелочноземельных металлов. Зонная структура бериллия приведена на рис. 14.15. Можно заметить, что зоны 2s и 2р, каждая из которых заполнена лишь частично, перекрываются. [2]
 |
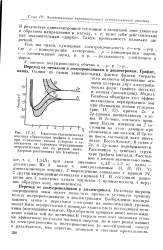
Возникновение запрещенной зоны вследствие требований симметрии. [3] |
При перекрывании зон, соответствующих различным атомным, орбиталям, могут возникнуть осложнения, поэтому предсказать, будет ли вещество обладать металлическими свойствами, не всегда л гко. Например, в случае магния могло бы показаться, что 3s - зона должна быть заселена полностью, так как имеется по два электрона от каждого атома. Однако Зр-уровень в отдельных атомах Mg находится настолько близко к Зз-уровню, что при сближении атомов Mg расширение энергетического уровня ( образование зоны) приводит к перекрыванию зон. Таким образом, имеются дополнительные энергетические уровни, доступные для электронов Mg, и может появиться электропроводность. Действительно, когда s - и р-зоны перекрываются, они теряют свою индивидуальность и результирующие уровни правильнее описывать как гибридные. [4]
 |
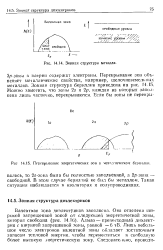
Возникновение энергетических зон кристалла из энергетических уровней атомов по мере их сближения. а - натрий. б - алмаз. [5] |
В кристаллическом натрии происходит перекрывание зон, образованных 3s - и 3 / 7-орбиталями. Для металлов первой группы это перекрывание не играет существенной роли, так как количество свободных орбиталей в s - зоне у них велико. Однако такое перекрывание s - и р-зон, наблюдаемое и для металлов второй группы периодической системы элементов, играет важную роль. Лишь глубокое перекрывание зон, образованных s - и р-орбиталями их атомов, сообщает металлические свойства кристаллам этих элементов. [6]
 |
Возникновение энергетических зон кристалла из энергетических уровней атомов по мере их сближения. а - натрий. б - алмаз. [7] |
В кристаллическом натрии происходит перекрывание зон, образованных 3s - и Зр-орбиталями. Для металлов первой группы это перекрывание не играет существенной роли, так как число свободных орбиталей в s - зоне у них велико. Однако такое перекрывание s - и р-зон, наблюдаемое и для металлов второй группы периодической системы элементов, играет важную роль. Атомы этих элементов имеют по два валентных s - электрона, следовательно, все орбитали в s - зоне их кристаллов будут полностью заполнены. Лишь глубокое перекрывание зон, образованных s - и р-орбиталями их атомов, сообщает металлические свойства кристаллам этих элементов. Образование зон проводимости в кристаллах d - элементов обычно сопровождается значительным перекрыванием ns - и ( - 1) а. Это значит, что перекрывание d - орбиталей в таких кристаллах невелико. [8]
Этому расстоянию соответствует возможность перекрывания зон, что влечет за собой гораздо более высокую электропроводность графита. [9]
При высоких концентрациях железа наблюдается перекрывание зон никеля, кобальта и меди. [10]
Но благодаря показанному на рисунке перекрыванию зон для возбуждения электронов в зону 2р - орбиталей необходима бесконечно малая энергия. [12]
 |
Услопня перокрынанин зон при сближении атомов металла ( и углэрода ( Ь. [13] |
На рис. 146, d показано перекрывание зон в случае типичного металла. [14]
Страницы: 1 2 3 4