Перекрывание - электронное облако
Cтраница 1
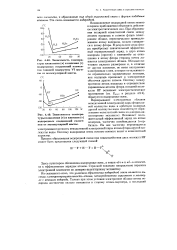
Перекрывание электронных облаков у производных аллильного и бензильного гомологических рядов вызывает также отчетливую активацию, что было показано Уинстейном на примере различных реакций сольволиза. [1]
 |
Схема различного взаимного расположения перекрывающихся р-облаков. Выделено положение с максимальной областью перекрытия. [2] |
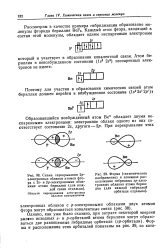
Перекрывание электронных облаков в соответствии со схемами 5, б на рисунке22 приводит к так называемой л-связи. При я-связи общее электронное облако пары связывающих электронов состоит из двух частей. Одна часть общего электронного облака лежит по одну сторону от оси, проведенной через ядра связанных атомов, другая часть этого облака находится симметрично по другую сторону от оси. Между этими частями проходит узловая плоскость с нулевой электронной плотностью. Таким образом, при я-связи связывающее электронное облако лежит не на линии связи, как при о-связи, а симметрично по обе стороны от этой линии. По обе стороны от линии связи находится и область перекрывания. [3]
Перекрывание электронных облаков Ру-электронов, образующих связь, соответствует новому распределению зарядов, которые сконцентрированы в двух областях, симметричных по отношению к оси х и расположенных соответственно над и под этой осью. [4]
Перекрывание электронных облаков неподеленной электронной пары фтора одной молекулы воды и орбитали водорода другой молекулы воды способствует образованию ковалентной связи по донорно-ак-цепторному механизму. Возникает положительный эффективный заряд на атоме водорода, частично освобождается ls-op - биталь. [6]
Области перекрывания электронных облаков заштрихованы. [8]
Степень перекрывания электронных облаков в случае ст-связи значительно превосходит перекрывание при л-связи. Поэтому а-связь обычно оказывается более прочной, чем л-связи. [9]
Области перекрывания электронных облаков заштрихованы. [11]
 |
Ковалентные связи, образующиеся в результате перекрывания электронных облаков. [12] |
Степень перекрывания электронных облаков в случае а-связи значительно превосходит перекрывание при я-связи. Поэтому а-связь обычно оказывается более прочной, чем л-связь. Например, в молекулах азота ( N N) и ацетилена ( Н - С С - Н) атомы азота и соответственно атомы углерода соединены одной а - и двумя л-связями. Энергии этих связей ( в эв на 1 связь) сопоставлены ниже. [13]
 |
Схема перекрывания электронных облаков. [14] |
Область перекрывания электронных облаков - это область высокого отрицательного заряда, который притягивает положительно заряженные ядра атомов. [15]
Страницы: 1 2 3 4 5