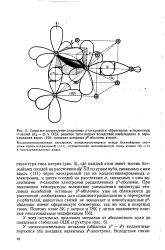
Перекрытие - р-орбиталь
Cтраница 1
Перекрытие р-орбиталей обусловливает основную ковалентную компоненту энергии решетки, присутствующую даже в ионных соединениях галогенидов щелочных металлов. В соответствии с концепцией электроотрицательности сдвиг и понижение зарядов на ионах тем сильнее, чем больше разность электроотрицательностей атомов неметалла и металла, Энергия решетки карбидов, нитридов и окислов складывается из ковалентной составляющей, обусловленной валентными а-связями перекрывающихся р-орбиталей и ионной, кулоновской связи возникающей вследствие притяжения ионов Ме и X, несущих небольшой эффективный заряд z, и действующей также вдоль валентных связей. [1]
 |
Схема перекрытия ор биталей для фрагментов Н Н. [2] |
Ранее рассматривались примеры резонанса ( сопряжения), связанные с перекрытием р-орбиталей. [3]
 |
Схема перекрытия р-орбиталей двух р-атомов с образованием двух я-связей, расположенных во взаимно перпендикулярных плоскостях. [4] |
Легко видеть, что вращение одного из атомов вокруг оси симметрии ( т-связи приводит, при наличии дублирующих я-связей, к постепенному уменьшению перекрытия р-орбиталей до полного исчезновения при повороте на 90, что соответствует разрыву соответствующей я-связи. [5]
Низкотемпературные модификации скандия, иттрия, лантана и актиния обладают гексагональными плотными упаковками ( табл. 38), что свидетельствует об эллипсоидальной форме ионов вследствие отсутствия перекрытия внешних р-орбиталей их ионов Ме3 с оболочками рв. Однако при высоких температурах вблизи температур плавления отделяются все внешние s - и d - электроны, вследствие перекрытия р-оболочек у скандия, иттрия, лантана проявляются высокотемпературные объемноцентрированные кубические модификации. Актиний также должен иметь высокотемпературную объемноцентрированную кубическую модификацию. [6]
Точно так же переходные металлы VI группы f - хром, молибден, вольфрам, имеющие внешнюю электронную конфигурацию р8 - dV, вследствие металлического взаимодействия коллективизированных шести валентных электронов с остовами и перекрытия расщепленных р-орбиталей внешних остовных р6 - оболочек образуют ОЦК структуры во всем диапазоне твердого состояния. Такую же ОЦК структуру по тем же причинам имеет высокотемпературная у-модификация урана. [7]
При понижении температуры вследствие уменьшения амплитуды тепловых колебаний остовные рв-оболочки уже не сближаются до расстояний, необходимых для спинового расщепления и перекрытия р-орбиталей, валентных связей не возникает и невозбужденные р6 - оболочки имеют сферическую симметрию, так же как в инертных газах. [9]
Таким образом, при a - 3 превращении кальция из 12 сильных и коротких металлических связей каждого атома со своими ближайшими соседями в ГЦК структуре, образующихся в результате перекрытия внешних 452-оболочек, в ОЦК решетке сохраняется восемь таких же связей, а вместо исчезнувших вследствие изменения координации атомов четырех металлических связей, возникает шесть новых более длинных ( аоцк 2d / J / 3 l 14d) и поэтому менее сильных ковалентных связей. Энергия 12 металлических связей в плотной кубической или гексагональной решетке приблизительно равна суммарной энергии восьми таких же металлических связей и шести более длинных ( на 14 %) более слабых ( приблизительно на 25 - 50 %) ковалентных связей, возникающих вследствие перекрытия расщепленных р-орбиталей остовных р6 - оболочек. Разность энергий ГЦК и ОЦК решеток равна теплоте полиморфного превращения: ДЯгцк-юцк 12 Ямет. [10]
 |
Фазовая диаграмма церия. [11] |
Это проявляется в отсутствие взаимодействия jo - орбиталей в ГЦК а-фазе и в перекрывании их только при высоких температурах вблизи точки плавления в области существования ОЦК структуры ( З - Yb. Плавление не приводит к изменению ОЦК конфигурации, и жидкость I имеет Кя &8. С повышением давления вследствие сближения ионов и усиления перекрытия р-орбиталей область ОЦК структур расширяется за счет ГЦК плотной а-фазы, которая исчезает при 41 кбар и 25 С. РГ-диаграммы европия, иттербия стронция и бария поразительно похожи, что еще раз указывает на правильность размещения Ей и Yb во Пс группе. [12]
Общность электронного строения переходных металлов IV-VI групп приводит, как было показано в гл. Причина ОЦК координации ОЦК металлов заключается в расщеплении и перекрытии р-орбиталей их внешних ос-товных оболочек. Валентные оболочки тугоплавких металлов III - - VI групп характеризуются наличием двух наиболее слабо связанных внешних з2 - электронов и одного - четырех сильнее связанных и более внутренних d () - электронов. Все внешние d, s - электроны в металлах I-VI групп коллективизированы. [13]
Повышение электронной плотности в шаровой s - зоне вокруг атома в четыре раза означает как бы сфероидизацию атомов в решетках щелочноземельных металлов. Высокая электронная плотность сферических s - зон подавляет спиновое расщепление и препятствует перекрыванию остовных р6 - оболочек, которое ответственно за образование ОЦК структур. Поэтому повышение электронной плотности в сферической s - зоне при переходе от щелочных ( s1) к щелочноземельным ( s2) металлам ведет к стабилизации плотных гексагональных структур у а - Ве, Mg, p - Sr и плотных кубических структур у а - Ca и a - Sr за счет подавления перекрытия р-орбиталей и ОЦК координации, свойственной щелочным металлам. [14]
Кристаллические структуры актиноидов ( см. табл. 39) также тесно связаны с особенностями их электронного строения. В результате взаимодействия с электронным газом эти ионы сближаются, но при низких температурах их р-орбитали не перекрываются и вследствие псевдосферической симметрии ионов упаковываются в плотную гра-нецентрированную решетку с небольшой тетрагональностью. При повышении температуры вследствие развития р-орбиталей может возникнуть обменное взаимодействие, результатом чего может быть появление объемно-центрированной кубической р-модификации. Его ионы ( Th4) имеют внешнюю ортогональную р - оболочку. При низких температурах при сближении ионов перекрытия р-орбиталей не происходит, ионы ведут себя как псевдосферические и в результате ненаправленного взаимодействия с электронным газом упаковываются в плотную кубическую структуру а-тория. Выше этой температуры возникают ортогонально направленные обменные связи, в результате чего появляется объемноцентрированная кубическая структура fi - тория, устойчивая до температуры плавления. Протактиний в связи с наличием внешней оболочки у его иона и устойчивым валентным состоянием Ра5, обусловливающим более высокую электронную концентрацию ( 5эл / атом), может иметь подобно ванадию, ниобию и танталу и по тем же причинам объемноцентрированную кубическую структуру. Фактически было найдено, что при 20 протактиний имеет ОЦ тетрагональную решетку. Тетра-гональность может быть обусловлена загрязнениями образца. [15]
Страницы: 1 2