Перемещение - фенильная группа
Cтраница 1
Перемещение фенильных групп, вероятно, проходит легче, чем алкильных групп. Пиролиз 2 2 2-трифенилдиазоэтана приводит с высоким выходом к трифенилэтилену [8], а 2-метил - 2-фенил-диазопропан ( V) при этом претерпевает в основном миграцию фе-нильной группы. [1]
Для пути ( IV) характерно обратимое перемещение фенильной группы в карбониевом ионе ( в) - ( г) - ( д), в результате которого меченые и немеченые фенильные остатки обезличиваются, что и было найдено. [2]
У додецилбензолсульфоната моющая способность понижается при перемещении фенильной группы из 2 в 5 положение, но в случае тридецил - и тетрадецйлбензолсульфонатов наблюдается обратная зависимость. В последнем случае внутренние изомеры обладают наилучшей моющей и пенообразовательной способностью. [3]
В соответствии с таким механизмом должно проходить перемещение фенильной группы. В случае изомеров 1-хлор - 1 2-дифенил-этилена а-отщепление, очевидно, невозможно. Иначе говоря, под действием фениллития преимущественно проходит г с-элиминирование. Можно предполагать, что причина этого состоит в некоторой координации атакующего основания и отщепляющегося хлора под влиянием катиона лития. Таким образом, для алкенилгалогенидов, имеющих р-водороды, - элиминирование исключается. [4]
У линейных алкилбензолсулъфонатов смачиваемость повышается по мере перемещения фенильной группы к середине алкильной цепи. Также она увеличивается с увеличением температуры и концентрации растворов, удлинением цепи до 12 атомов углерода. Удлинение алкильной цепи свыше 12 атомов углерода ведет к уменьшению смачиваемой способности вещества. Разветвленные алкилбенэолсуль-фонаты - лучшие смачиватели, и эта способность у них возрастает при увеличении длины алкильной цепи от 9 до 16 атомов углерода, а также при перемещении фенкльной группы к середине алкильной цепи. [5]
Считают, что эта перегруппировка инициируется нуклеофильной атакой пидроксил-ионом углерода карбонильной группы с образованием аниона, который перегруппировывается с перемещением фенильной группы. Движущей силой этой реакции является образование карбо-новой кислоты, стабилизованной резонансом. [6]
Считают, что эта перегруппировка инициируется нуклеофильной атакой гидроксил-ионом углерода карбонильной группы с образованием аниона, который перегруппировывается с перемещением фенильной группы. Движущей силой этой реакции является образование карбо-новой кислоты, стабилизованной резонансом. Бензиловая кислота легко окисляется в кислом растворе, например, бихроматом калия с серной кислотой и превращается при этом в бензофенон и двуокись углерода. [7]
С другой стороны, при сольволизе ариловых эфиров р-фенил-этанола в водных и спиртовых средах практически не наблюдается перегруппировок с перемещением соседней фенильной группы, поскольку в этих средах возникающий положительный заряд стабилизируется заметным нуклеофильным участием растворителя. [8]
Перегруппировка обусловливается очень большим С-эффектом этрицательно заряженного атома кислорода: происходит образова ние двойной связи между кислородом и углеродом и перемещение фенильной группы вместе с электронной парой связи к соседнему углеродному атому; в конечном итоге образуется карбоксильная группа. [9]
В первом случае происходит обычная валентная изомеризация ( изменилось только число л - и сг-связей), во втором в процессе превращения происходит перемещение фенильной группы. [10]
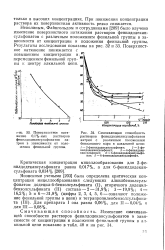 |
Смачивающая способность растворов фенилдодекансульфонатов натрия с различным положением бензольного ядра в алкильной цепи. [11] |
Неволиным, Файнгольдом и сотрудниками [209] было изучено изменение поверхностного натяжения растворов фенилдодекан-сульфонатов с различным положением фенильной группы в зависимости от концентрации и положения фенильной группы. Поверхностное натяжение понижается с повышением концентрации и перемещением фенильной группы к центру алкильной цепи. [12]
Критическая концентрация мицеллообраэования зависит от строения углеводородного радикала молекулы ПАВ. Для алкилбензол-сульфонатов: с увеличением углеводородного радикала ККМ уменьшается, разветвление алкильного радикала и перемещение фенильной группы к середине цепи приводит к увеличению ККМ. Введение в раствор небольшого количества длинноцепочсчных спиртов значительно понижает порог ККМ. [13]
Эти данные указывают на присутствие С14 в карбоксильной группе фе-нилуксусной кислоты. Авторы работы считают, что фенилуксусная кислота образуется не только по механизму окисления-восстановления, но и путем перемещения фенильной группы. Доля последней реакции невелика. [14]
Исходя из анизальциклогексана ( I), авторы получают при действии перекиси бензойной кислоты этиленоксид ( II), который превращается путем перегруппировки, сопровождаемой расширением кольца, в анизилциклогептанон ( III), причем изомеризация эта в сущности аналогична уже разобранной нами выше, на стр. Если же при проведении аналогичных реакций применить в качестве исходного продукта бензальциклогек-сан ( R-фенил), то в результате не происходит расширения кольца, а получается фенилциклогексилформальдегид, так как образование карбонильной группы осуществляется в этом случае путем перемещения ароматического остатка. И наконец, если, исходить из фенилциклогептена ( IV), получится этиленоксид, обладающий формулой ( V), то это соединение претерпевает частично изомеризацию и превращается путем сужения кольца в фенилциклогексилформальдегид ( VI); наряду с этим имеет место, однако, также и образование фенилциклогептенона, которое не связано с изменением кольцевой системы, но сопровождается перемещением фенильной группы. В тех случаях, когда R-анизил, последняя из перегруппировок протекает еще легче. [15]
Страницы: 1 2