Чистый бор
Cтраница 3
Бор легко соединяется с фтором, хлором, бромом и иодом. Чистый бор не взаимодействует с хлором при температурах ниже 500, но быстро соединяется с ним при 550, образуя трихлорид бора. В соляной и плавиковой кислотах Гюр не растворяется даже при кипячении. Тонкоизмельченный бор окисляется горячей концентрированной азотной кислотой, тогда как с компактным металлом эта реакция протекает очень медленно. Горячая концентрированная серная кислота или горячий раствор хромовой кислоты в серной кислоте почти не действуют на бор. Бор растворим в смеси азотной, соляной и серной кислот. [31]
В этих процессах получается аморфный бор, загрязненный примесями. Более чистый бор получают восстановлением его хлорида водородом или осаждением кристаллического бора на раскаленной проволоке из тантала или вольфрама. [32]
В этих процессах получается аморфный бор, загрязненный примесями. Более чистый бор получают восстановлением его хлорида водородом или осаждением кристаллического бора на раскаленной проволоке из тантала или вольфрама. Они более экономичны вследствие сравнительно меньшей стоимости исходного продукта и низких температур проведения процесса. [33]
В чистом кислороде при 1000 окисление протекает очень быстро. Мелкие частицы чистого бора размером 0 1 - 10 мк при комнатной температуре окисляются медленно. Например, при анализе образца, первоначально содержавшего 99 % бора, после хранения в течение нескольких месяцев в лаборатории было найдено только 92 % бора. При увеличении размеров частиц стойкость против окисления также возрастает. В случае частиц с размерами не меньше 40 меш никаких изменений состава не наблюдается. Поэтому тонкоизмельченный чистый бор следует хранить в заполненных герметичных контейнерах. [34]
Совокупность полученных экспериментальных данных подтверждает гидрофильность технического бора, и притом тем большую, чем чище образец бора. Повышенная гидрофильность более чистого бора связана с технологией обогащения бора2, приводящей к повышению степени окисленности поверхности его частиц. Образующиеся пленки оксидов обладают высокой гидрофильностью. [35]
Почему таким путем трудно получить чистый бор. [36]
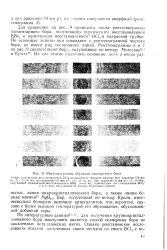 |
Рентгенограммы образцов дисперсного бора. [37] |
Для сравнения на рис. 9 приведены также рентгенограммы элементарного бора, полученного термическим восстановлением ВВг3 и термическим восстановлением9 ВС1, в кварцевой трубке. По основным линиям они совпадают с рентгенограммой чистого бора, но имеют ряд посторонних линий. [38]
По данным химических анализов, нитрид бора при испарении обогащается чистым бором. Так, при длительных опытах были получены образцы, содержащие 90 - 95 % чистого бора. [39]
С помощью магния обычно и получали в лаборатории бор из природного ангидрида. Правда, образующийся по этому методу элементарный бор очень загрязнен примесями, а потому за последнее время были разработаны новые способы получения чистого бора, содержащего не более 0 01 % примеси, что существенно для применений его в качестве полупроводника. [40]
Имеет значение также использование бора и его соединений как восстановителей и гидрирующих агентов для вулканизации каучука и как катализаторов процессов полимеризации. Особый интерес представляет проблема замены изоляционных, смазочных, эластических и пластических органических материалов новыми, выдерживающими без разрушения более высокую температуру, высокомолекулярными веществами, содержащими вместо углерода или наравне с ним В, N, S, Р и Si. Чистый бор а также нитрид и карбид бора применяются как экраны, поглощающие нейтроны, и как замедлители ядерных процессов. [41]
Борная кислота содержится в воде некоторых горячих источников. В СССР месторождения борных руд находятся в Казахской ССР. Чистый бор получают из борного ангидрида В203 восстановлением его металлами: натрием или магнием. Бор может существовать в кристаллическом и аморфном состояниях. [42]
Бор при обыкновенной температуре инертный металл; он не реагирует с водой, не окисляется на воздухе и не соединяется с другими элементами. Бор легко соединяется со фтором, хлором, бромом и иодом. Чистый бор не взаимодействует с хлором при температурах ниже 500 С, но быстро соединяется с ним при 550 С, образуя трихлорид бора. В соляной и плавиковой кислотах бор не растворяется даже при кипении. Бор окисляется в горячей азотной кислоте, однако горячая концентрированная серная кислота и горячий раствор хромовой кислоты в серной кислоте на бор почти не действуют. Бор растворяется в смеси азотной, соляной и серной кислот. [43]
При этом выделяется аморфный бор, который перекристаллизацией в расплавленных металлах можно перевести в кристаллическое состояние. Однако этот метод дает продукт, загрязненный примесями. Более чистый бор ( 99 5 %) получается электролизом расплавленных фторобо-ратов. [44]
В литературе описан ряд способов получения элементарного бора. По этому способу при тщательном проведении процесса в атмосфере ведорода получается 91 - 93 % - ный бор, а при дополнительной очистке-продукт с более высоким содержанием бора. Более чистый бор может быть получен восстановлением галогенидов бора водородом. Впервые этот метод был применен Вайнтраубом3 4, использовавшим для восстановления хлористого бора дуговой разряд между медными электродами. [45]
Страницы: 1 2 3 4