Перенос - противоион
Cтраница 1
Перенос противоиона составляет главное содержание электрического движения ионов-в процессе; противоионы в результате электроэсмоса переносят с собой определенное количество воды. [1]
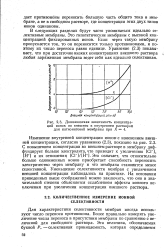 |
Доннановская зависимость концентраций ионов во внешнем и внутреннем растворах для катионитовой мембраны при X 4. [2] |
Для характеристики селективности мембран иногда используют число переноса противоиона. Более правильно измерять увеличение числа переноса в присутствии мембраны по сравнению с величиной для свободного раствора. [3]
 |
Принцип эпектропиза с использованием ионообменных мембран. [4] |
Чем выше обменная емкость, тем легче осуществляется перенос противоионов ( ионов натрия) и тем выше электропроводность мембраны. [5]
Проникновение одноименных ионов в мембрану не только понижает числа переноса противоионов, но проводит к тому, что мембрана становится проницаемой для диффузии электролита. [6]
За основу были приняты лимитирующие значения наиболее важных свойств мембран: число переноса противоиона в 0 3 N растворе хлористого натрия больше 0 93; электропроводность при 30 С, в 0 1 N растворе хлористого натрия больше 60 мом-1 - см-2; поток свободной диффузии через мембрану, помещенную между 1 5 % - ным раствором хлористого натрия и водой, при 30 С меньше 1 5 - 10 мэкв / смг-сек. [7]
На ранней стадии разработки синтетических ионитовых мембран Деви и Джилиланд [ All, IP3J предложили использовать преимущественный перенос противоиона через ионитовые мембраны для разделения ионов в системе, напоминающей дистилляционную колонну. [8]
Мы здесь не будем применять эту систему анализа, так как независимый межфазный перенос воды в рамках анализа изотермы ионного обмена требует рассмотрения переноса десольватированных противоионов, что вызывает определенные затруднения при использовании таких моделей для расчета. Естественно, что разделение воды на приносимую с сольватированными ионами и независимо переносимую воду, сольватирующую матрицу ионитов, при термодинамическом анализе недопустимо. [9]
На основании выполненных экспериментов можно сделать вывод о том, что подъем тока на третьем участке поляризационной кривой ( рис. 2) связан по-прежнему с переносом противоионов электролита. Механизм их подвода к мембране в условиях, когда диффузия уже не может обеспечить достаточно высокую концентрацию в пленке около мембраны, различными авторами объясняется по-разному. [10]
Перенос растворителя в результате конвекции жидкости, содержащейся в порах, при наличии электрического тока называется электроосмосом. Поскольку числа переноса противоионов уменьшаются с увеличением концентрации раствора, электрическая продуктивность также уменьшается. По этой причине деминерализация путем электродиализа более экономична для случая разбавленных растворов. Однако, если растворы являются сильноразбавленными ( 200 - 400 мг / л NaCl), сопротивление раствора будет слишком высоким для энергетически эффективного разделения. Накопление электролита в одном отсеке и истощение в другом противодействуют переносу вследствие увеличения противодействия за счет диффузии. Перенос электрического тока пропорционален плотности тока и не зависит от толщины мембраны. Поскольку скорость противодействующей диффузии обратно пропорциональна толщине мембраны, при использовании таких мембран и высокой плотности тока эффективность процесса должна возрастать. Эти два условия обусловливают более высокое напряжение и более высокие омические потери вследствие выделения теплоты. Кроме того, если плотность тока превышает некоторое критическое значение, выход по току резко снижается. [11]
 |
Электрохимическая новка для обессоливания Лугов-2. [12] |
В ионообменной мембране, погруженной в разбавленный раствор какого-либо электролита, практически единственными переносчиками тока служат противоионы. Поэтому в разбавленных растворах число переноса противоионов через мембрану близко к единице. Возникающая при этом концентрационная поляризация подобна той, которая имеет место на электродах. [13]
Тассмотрим механизм ионного обмена с точки зрения кинетики. При обмене между двумя фазами происходит перенос противоионов в обеих фазах к поверхности раздела и от нее. Этому переносу ионов в растворе способствует его перемешивание. Толщина пленки примерно 10 - 3 - 10 - 2 см. Процесс обмена, происходящий между зернами ионообменника и хорошо перемешиваемым раствором, сводится к трем последовательным стадиям: I - диффузия обменивающихся противоионов через стационарную пленку, окружающую зерно ионообменника; II - диффузия их в зерне ионообменника; III - химический обмен. Собственно обмен - стадия III - протекает практически мгновенно, поэтому ионный обмен рассматривают как чисто диффузионный процесс, скорость которого определяется самой медленной стадией: либо диффузией в пленке - пленочная кинетика, либо диффузией в зерне - гелевая кинетика. Все факторы, которые увеличивают диффузионный поток в пленке и уменьшают поток в зерне, способствуют гелевой кинетике; пленочной кинетике благоприятствуют факторы, увеличивающие диффузионный поток в зерне и уменьшающие его в пленке. Например, диффузия в пленке может быть скоростьопределяющей стадией в системах с более высокой концентрацией фиксированных ионов, с меньшим числом поперечных связей в матрице ионообменника. [14]
А в замкнутой цепи происходит растворение цинка на аноде, осаждение меди на катоде и перенос жидкосги слева направо, как указано стрелкой. Таким образом, направление переноса жидкости во всех случаях совпадает с направлением переноса противоионов. Все это указывает на то, что во внутренней цепи гальванического элемента, образованной пористым телом, может происходить электроосмотический перенос норового раствора даже при малых градиентах напряжения электрического поля. [15]
Страницы: 1 2