Перенос - реагент
Cтраница 3
Член, содержащий коэффициенты активности, представляет собой совокупную свободную энергию переноса реагентов и продуктов раек - ции из реальной среды в стандартное состояние. Если в качестве константы равновесия используется Кс, то это значит, что в качестве стандартного принято как раз то состояние, в котором проводится эксперимент; тогда - RT nKc - стандартное изменение свободной энергии для данной среды. Индексы а и с обычно опускают; поэтому, чтобы понять, какое состояние принято за стандартное, требуется более детальное рассмотрение литературных данных по константам К. [31]
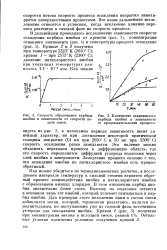 |
Скорость образования карбида ниобия в зависимости от скорости подачи смеси.| Количество всадившегося карбида ниобия в зависимости от продолжительности процесса. [32] |
Все наши дальнейшие исследования относятся к условиям, когда исключено влияние переноса реагентов в газовой фазе на скорость процесса. [33]
Химическая кинетика посвящена изучению реакций в отрыве от осложнений, вносимых особенностями переноса реагентов и тепла в реакторе. [34]
В процессе, идущем на пористом катализаторе, наряду с диффузионным сопротивлением переносу реагентов внутрь зерна могут возникнуть и затруднения с отводом тепла реакции. Перенос тепла в зерне идет по двум механизмам: 1) за счет теплопроводности твердой пористой частицы и 2) вследствие молекулярной диффузии в порах. Если материал пористого зерна хорошо проводит тепло, частица катализатора при всех условиях остается изотермической. В случае же малой теплопроводности катализатора механизм тепло - и массопереноса в зерне один и тот же, и надо ожидать одновременного появления градиентов концентраций и температур в частице по мере перехода реакции во внутридиффузионную область. [35]
Наилучшие результаты для получения циклопропанкарбоновой кислоты достигаются при использовании межфазного катализа с переносом реагентов нз водной в органическую фазу с помощью хлорида триэтилбензиламмония или N ( C4Hg) 4 Br при взаимодействии одного моля малонового эфира и одного моля 1 2-дибромэтана. [36]
Это объясняется тем, что реакция в целом складывается из двух стадий - переноса реагентов через поверхность раздела и собственно химического превращения. [37]
В реакциях, протекающих на твердой поверхности, области осуществления химического превращения и переноса реагентов разграничены в пространстве. Если скорости этих процессов существенно различны, то может оказаться, что скорость расходования исходного вещества определяется не скоростью химического превращения, а скоростью переноса реагентов. [38]
С теоретической точки зрения проблема концентрационной поляризации весьма близка к общей проблеме о переносе реагентов к поверхности реакции в случае любой гетерогенной реакции в растворе, хотя явления, протекающие с участием ионов, обладают своими специфическими особенностями, которые будут указаны ниже. [39]
Уравнение ( 32) показывает, что скорость процесса переноса заряда равна сумме скоростей переноса реагента к поверхности и рао ходования поверхностного избытка реагента на границе. Аналогична та же величина равна Сумме скорости переноса продукта реакции от поверхности и скорости образования поверхностного избытка продукта. [40]
Такой подход оправдан в тех случаях, когда ток не лимитируется заметно за счет переноса реагентов к электродам. Тогда концентрации практически постоянны и уравнение ( 76 - 3) применяется с практически постоянной проводимостью. Такое обоснование уравнения Лапласа значительно отличается от утверждения о том, что уравнение Лапласа возникает из условия электронейтральности. Можно ожидать, что описанная здесь процедура приведет к некоторым несогласованностям, если в дальнейшем пытаться исследовать детальное поведение каждого типа компонентов в растворе вблизи электродов. [41]
Для систем с хим р-циями на характер распределения частиц большое влияние оказывает соотношение между характерными временами переноса реагентов и их хим. превращения. Если скорость хим. превращения мала, распределение частиц не сильно отличается от случая, когда р-ция отсутствует. Если скорость р-ции велика, ее влияние на характер распределения частиц велико и использовать средние концентрации частиц ( т.е. ф-ции распределения с п - 1), как это делается при использовании закона действующих масс, нельзя. [42]
 |
Межфазный катализ. [43] |
Механизм действия катализаторов этого типа наиболее наглядно иллюстрируется примером, показанным на рис. 3.7. Межфазные катализаторы осуществляют перенос реагентов между органической и водной фазами, обеспечивая контакт между реагентами и тем самым возможность протекания реакции. [44]
В соответствии с этой особенностью для реакций гетерогенного типа различают так называемые диффузионную область протекания реакции, определяемую переносом реагентов, и кинетическую область, определяемую превращением реагентов на поверхности. [45]
Страницы: 1 2 3 4